El modelo atómico. Parte I: del origen del concepto al modelo de Rutherford y el descubrimiento de los isótopos

El modelo atómico representa una de las ideas más poderosas de la historia de la ciencia: la noción de que toda la materia que nos rodea —desde una roca hasta una estrella, desde el agua que bebemos hasta nuestro propio cuerpo— está formada por unidades diminutas llamadas átomos. Sin embargo, esta imagen, que hoy parece casi evidente, es el resultado de un largo recorrido intelectual lleno de preguntas, errores, intuiciones brillantes y experimentos decisivos. Entender cómo hemos llegado a concebir el átomo permite conocer mejor la estructura íntima de la materia, y representa una de las aventuras más fascinantes del pensamiento científico.
El átomo. El origen del término
La palabra átomo, proviene del latín atŏmus , y esta a su vez del griego clásico, ἄτομος (átomos, "indivisible"). Hoy sabemos que aquello a lo que llamamos átomo no es indivisible; es más, algunas de las partículas que componen el átomo tampoco lo son. Que esta palabra provenga del griego, no es casualidad, pues ya en la antigua Grecia se teorizó sobre este concepto de unidad elemental que conforma la materia. Sin embargo, durante mucho tiempo predominaron muchas teorías elementales que formulaban que los constituyentes de la materia eran: al agua, la tierra, el fuego y el aire, y en algunos casos la quintaesencia o éter.
En occidente, la teoría de los cuatro elementos tuvo su origen en la filosofía presocrática, que tuvo comienzo en el siglo VI a.C. con los tres miembros de la escuela de Mileto: Tales, Anaximandro y Anaxímenes. Para ellos el origen (arché o arqué) del mundo era atribuido al agua, el Ápeiron (lo ilimitado) y el aire, respectivamente. Heráclito por su parte propuso el fuego. Otros como Jenófanes consideraban la tierra como el origen, mientras que otros como Pitágoras, lo atribuían a los números, exponiendo que el número como tal no era un ente abstracto sino algo real, la más real de las cosas, y por ello era el elemento constituyente de ellas. No obstante, no todas las corrientes de pensamiento se nutrían del monismo, filósofos de la época como Parménides alertaron de la dificultad de explicar toda la diversidad del universo con un único origen, y tras este argumento afloró el pluralismo. Uno de los más destacados pluralistas fue Empédocles (495-435 a.C.) quien postuló que eran cuatro los principios materiales (raíces) de la realidad: fuego, tierra, aire y agua. Los siguientes versos de Empédocles emplean una designación divina para los diferentes elementos:
“Escucha, primero, las cuatro raíces de todas las cosas: Zeus brillante, Hera dadora de vida, Aidoneo y Nestis, que con sus lágrimas hace brotar la fuente mortal”
La Croce, Ernesto: Los Filósofos Presocráticos
Aunque siempre ha habido polémica en cuanto al elemento designado para cada divinidad, historiadores como Guthrie han mostrado sus creencias al respecto: Zeus: fuego, Hera: aire, Aidoneo: Tierra y Nestis: agua

Destacar, que en este escenario, ningún elemento destaca sobre otro, o es anterior al resto.
Como muchos otros pensadores de la época, Empédocles creía en el concepto Panta rei, que establece que todo fluye, una doctrina de flujo perpetuo.
“Todo se mueve y nada permanece y en el mismo río no nos bañamos dos veces.”
Platón, Crátilo
Como estos elementos están sometidos a un cambio constante, se incorporan dos fuerzas activas: la Amistad y el Odio, que infunden movimiento a los elementos. La Amistad tiende a unir, mientras que el Odio tiende a desunir. Además, Empédocles ofrece una concepción cíclica del universo y estas fuerzas activas son las que determinan los estadios de dicho desarrollo cíclico.
Estos cuatro elementos de Empédocles son adoptados también en una de las principales obras de Aristóteles (384-322 a.C.), Metafísica. Aristóteles añadió a la teoría de Empédocles, cuatro cualidades: húmedo y seco, caliente y frío.
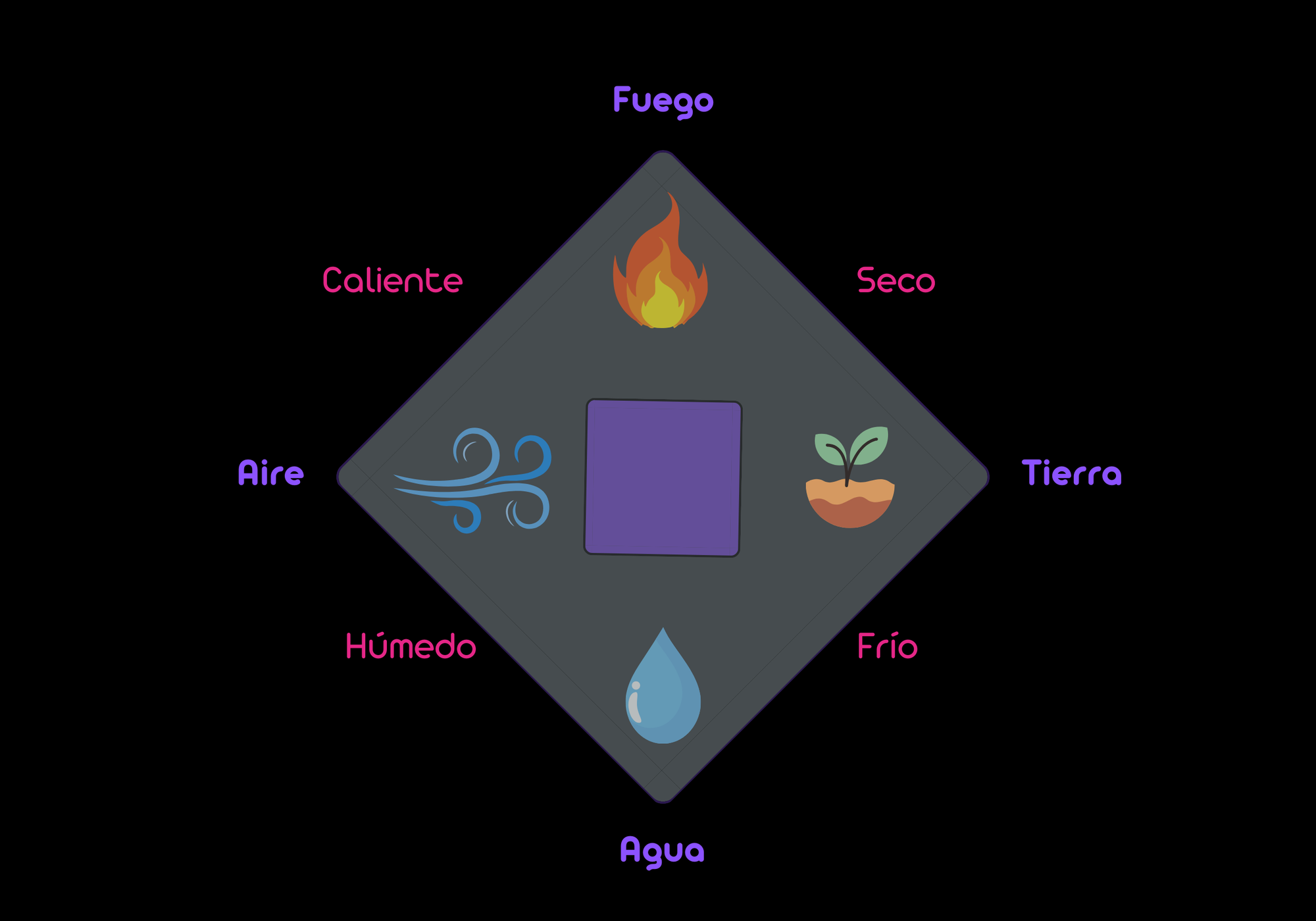
Esta teoría de los elementos aristotélica tuvo una gran aceptación y ha sido muy influyente durante siglos en occidente, pues no cae en desuso hasta el Renacimiento, con la consolidación del paradigma científico.
La teoría atómica, surge como concepto filosófico en la antigüedad, y nace con independencia en Grecia e India. Los más destacados filósofos atomistas de la antigüedad fueron Demócrito y Leucipo (siglos v y iv a.C.).
Demócrito, y su mentor, Leucipo, postulan los siguientes principios básicos para su teoría atómica:
- Los átomos son físicamente indivisibles, eternos y homogéneos.
- Entre cada átomo hay un espacio vacío.
- Los átomos son indestructibles.
- Los átomos están continuamente en movimiento.
- Hay diferentes tipos de átomos, aunque son diferentes únicamente en su forma y tamaño, no en sus cualidades internas.
- Las propiedades de la materia varían en función del agrupamiento de los átomos.

Pese a que hay diferencias notables entre el modelo actual y el de Demócrito y Leucipo, cabe mencionar que el punto de vista que adoptaron tiene fuertes semejanzas con el de la ciencia moderna, y esquivaron algunos axiomas que fueron sostenidos por diferentes escuelas y corrientes de pensamiento durante siglos. No sólo hay que reconocer su mérito por plantear el concepto de átomo, sino también por el hecho de teorizar el concepto de vacío y el de la inercia, conceptos que toman especial importancia en la ciencia de nuestros días.
Por desgracia, esta teoría atómica, que llegó a contar con cierto respaldo entre los pensadores de la época, fue condenada al olvido durante más de dos mil años. No es hasta el siglo XIX cuando se retoma el concepto y surge el primer modelo atómico con bases científicas, el modelo atómico de Dalton. Durante los próximos dos siglos los diferentes modelos atómicos se irán abriendo paso hasta el modelo mecánico cuántico actual. La física teórica y experimental se alinean, para dar lugar a principios del siglo XX a la formulación de la mecánica cuántica, que junto con el enfoque relativista arroja luz sobre la fenomenología del átomo, así como de su núcleo, y de las partículas elementales.
Historia de los modelos atómicos y origen de la tabla periódica
Año 1789: Tabla de elementos de Lavoisier
Si bien podemos considerar que Demócrito y Leucipo eran unos visionarios para su época, sus postulados no eran más que conjeturas, imposibles de contrastar con la tecnología del momento. Por lo tanto, el posicionamiento entre las diferentes teorías coexistentes se debe a cuestiones filosóficas fundamentalmente. Además, cabe destacar que los mecanismos de asociación y disociación de los átomos, según Demócrito y Leucipo, se debía a acciones mecánicas. En oposición a esto, Dalton, a la luz de los experimentos llevados a cabo por Lavoisier sobre la descomposición del agua mediante electrolisis, consideraba que el enlace entre los átomos era de naturaleza eléctrica. Previamente, en 1733 Bergmann sienta las bases del análisis químico, y en 1766 Cavendish consigue aislar al hidrógeno. En 1789 Lavoisier clasifica los elementos conocidos hasta entonces.

Ley de proporciones definidas
Estos resultados de Lavoisier, junto con la ley de las proporciones definidas en las reacciones químicas, enunciada en 1799 por Joseph-Louis Proust, llevaron a Dalton a formular la teoría atómica hacia 1808.

Año 1808: Modelo atómico de Dalton
Dalton enumeró cinco puntos principales para su teoría atómica:
- Los elementos están constituidos de partículas diminutas llamadas átomos que son indestructibles e indivisibles.
- Todos los átomos de un determinado elemento son idénticos.
- Los átomos de un elemento son diferentes de los de cualquier otro elemento, y los átomos de elementos diferentes se pueden distinguir unos de otros por sus respectivos pesos atómicos relativos.
- Los átomos de un elemento se combinan con los átomos de otros elementos para formar compuestos químicos, y un compuesto dado siempre tiene el mismo número relativo de tipos de átomos.
- Los átomos no se pueden crear ni dividir en partículas más pequeñas, ni se destruyen en el proceso químico. Una reacción química simplemente cambia la forma en que los átomos se agrupan.

Además, propuso «un principio de máxima simplicidad», que podría considerarse una suposición fruto de la fe en la simplicidad de la naturaleza:
Cuando los átomos se combinan siempre en la misma proporción, «... se debe presumir que forman una unión binaria, a menos que haya una razón de peso para suponer lo contrario».

El átomo de Dalton cumplía con las siguientes características:
- Esférico
- Macizo
- Indestructible
- Indivisible
Modelo de “bola de billar”

Dalton supuso que el hidrógeno era el elemento más ligero, por lo que introdujo el término masa atómica relativa como relación entre la masa de un átomo del elemento y la masa de un átomo de hidrógeno.
En su obra Nuevo sistema de Filosofía Química, Dalton identifica algunos átomos y moléculas sencillas. Nótese la escasez de elementos registrados en la época:
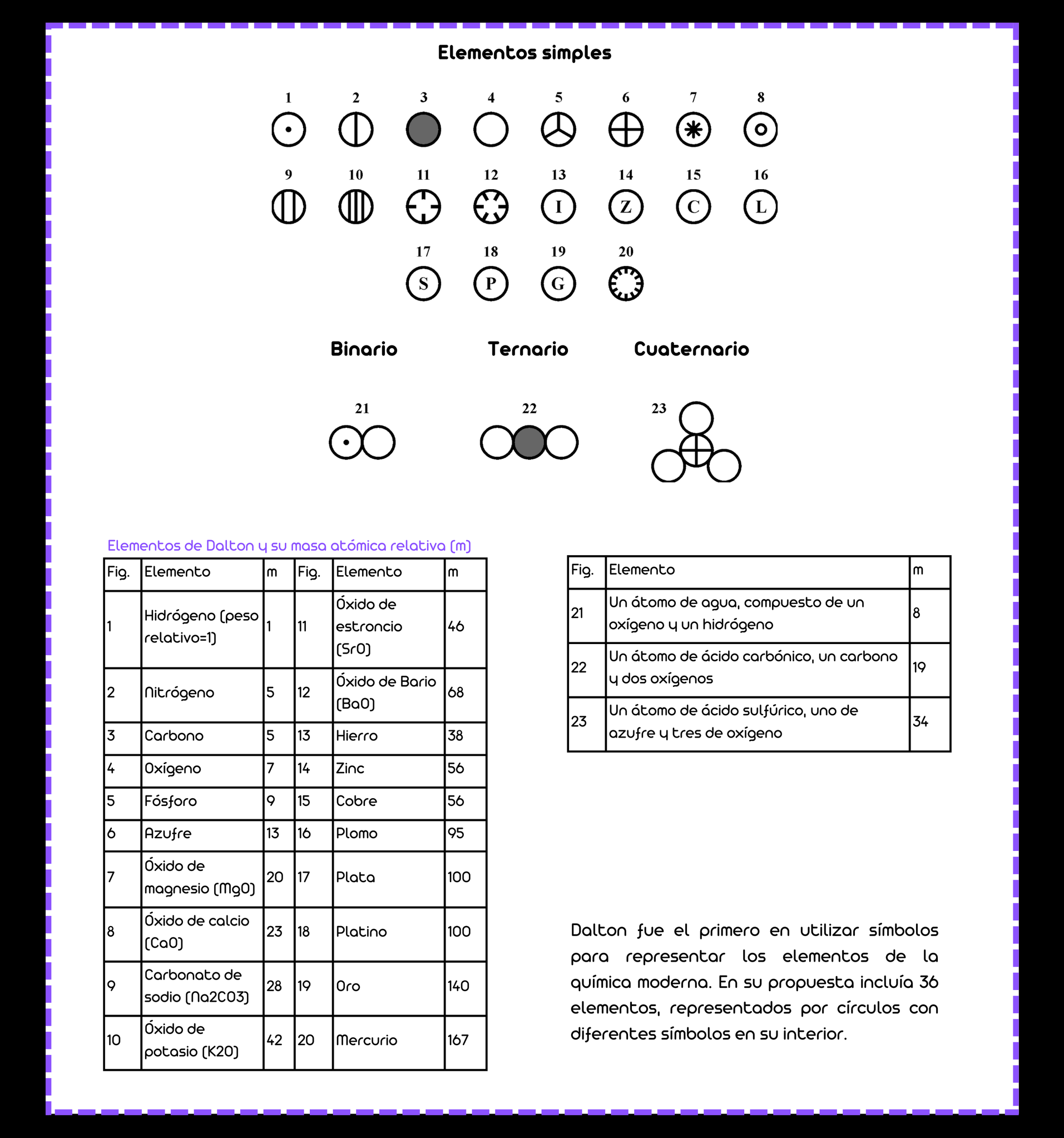
Año 1813: Tabla de los elementos de Berzelius
El sistema actual de símbolos químicos, basado en la primera letra (y con el tiempo una más) del nombre en latín del elemento, fue introducido en 1813 por el químico sueco Jöns Jacob Berzelius. Simplificó el sistema de Dalton, y organizó 47 elementos. En 1818, tras diez años de pruebas con más de 2.000 compuestos, también publicó las masas atómicas de los elementos que, para la época, eran asombrosamente precisas. Berzelius consideraba que el oxígeno era una unidad mucho más adecuada que el hidrógeno, por lo que calculó las masas atómicas relativas de los elementos estableciendo el peso del oxígeno exactamente igual a 100.
Hoy en día, seguimos usando muchos de ellos, pero el diseño moderno de la tabla periódica se debe al químico ruso Dimitri Mendeleyev, que presentó su tabla de 63 elementos organizados por masa atómica en 1869.

Año 1817: Ley de Tríadas
También cabe comentar las contribuciones de Johann Wolfgang Döbereiner (1780-1849), químico alemán cuyos descubrimientos fueron importantes para el desarrollo de la tabla periódica, y que en cierta manera sentaron las bases para la organización de los elementos en función de sus propiedades. Döbereiner observó ciertas tendencias en determinados grupos de elementos.

Entre sus observaciones, descubrió similitudes en la masa atómica de los siguientes grupos de elementos:
- Litio, potasio y sodio
- Calcio, estroncio y bario
- Azufre, selenio y telurio
- Cloro, bromo y yodo.
Tras estas observaciones intentó vincular las propiedades químicas de estos grupos, así como de sus compuestos, con los pesos atómicos. En su conocida Ley de Tríadas (1817), que podríamos identificar como una versión temprana de la tabla periódica, establece que cuando se ordenan los elementos en tríadas, el peso atómico central es aproximadamente igual al promedio de los pesos atómicos de los otros dos elementos. Este hallazgo permitió predecir las propiedades de elementos aún no descubiertos en ese momento.

En torno a 1850 los químicos llegaron a identificar unas veinte tríadas. Aunque supuso un avance, se descartó esta forma de agrupar los elementos ya que había algunos elementos que no cumplían las tríadas.
Año 1862: Tornillo telúrico
En 1862, el geólogo francés Alexandre-Émile Béguyer de Chancourtois plantea una clasificación periódica de los elementos basada en un sistema denominado tornillo telúrico.

En un cilindro dibujó una hélice con un ángulo de 45º, y sobre ella fue ubicando los elementos en función de creciente peso atómico, de modo que la línea vertical (generatriz) del cilindro interseca a los elementos con propiedades semejantes.
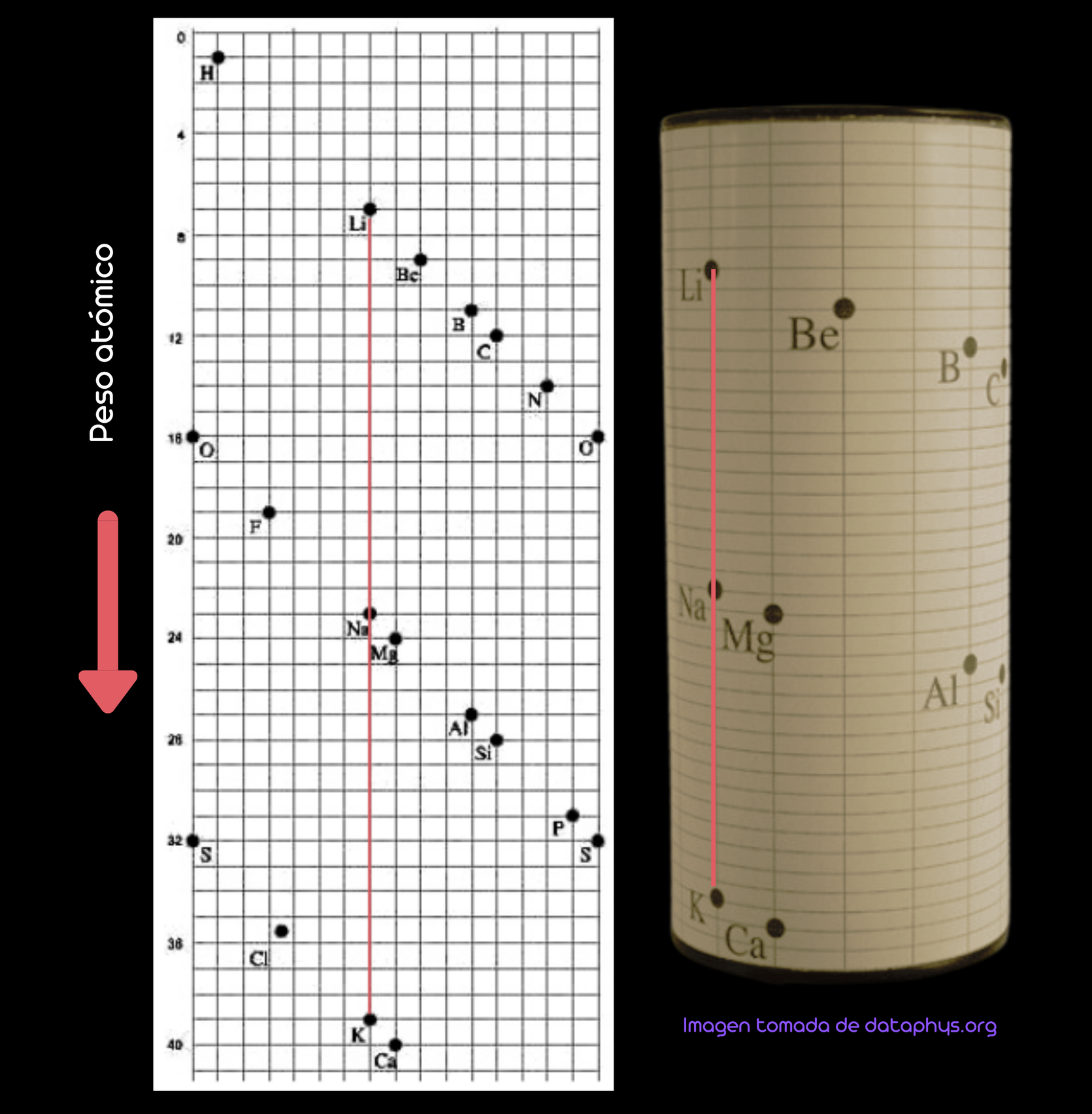
Como se puede apreciar en la imagen del tornillo telúrico, si trazamos una vertical podemos agrupar a diversos elementos atendiendo a la similitud de su naturaleza:
- Li (litio), Na (sodio) y K (potasio)
- Be (berilio), Mg (magnesio) y Ca (calcio)
- B (boro) y Al (aluminio)
- etc.
Año 1864: Ley de octavas / Valencia
A mediados del siglo XIX, se observó que cuando los elementos se organizan en orden de masas atómicas crecientes, las propiedades químicas parecen repetirse cada ocho elementos.

Esto llevó en 1864 a que John Newlands propusiera la denominada Ley de las Octavas. Este patrón se asemejaba a la repetición de notas musicales en una octava, de ahí su nombre.
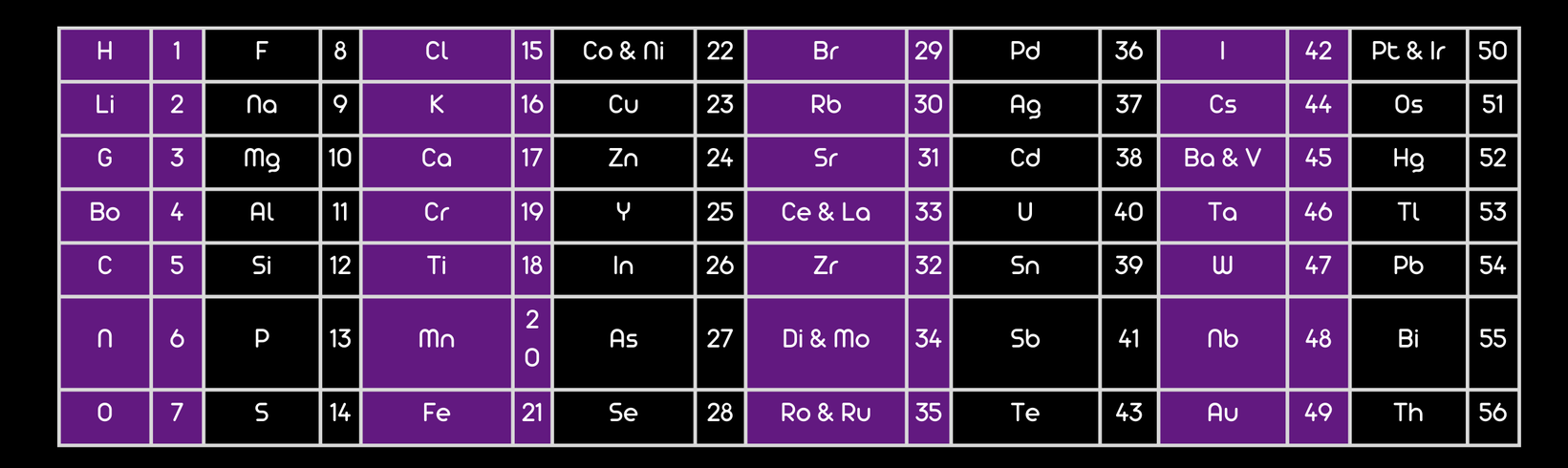
Conviene destacar que en esa época los gases nobles no habían sido descubiertos. Esta familia de gases inertes, denominados posteriormente gases nobles estaba formada por el helio, el neón, el argón, el kriptón y el xenón.
Conviene subrayar que la limitación principal era que sólo era aplicable para algunos de los elementos conocidos, por lo que la ley no era del todo fiable para todos los elementos. De hecho, Newlands sólo pudo aplicar su ley a los primeros 56 elementos, y tras eso, el patrón de las propiedades químicas dejaba de ser consistente.
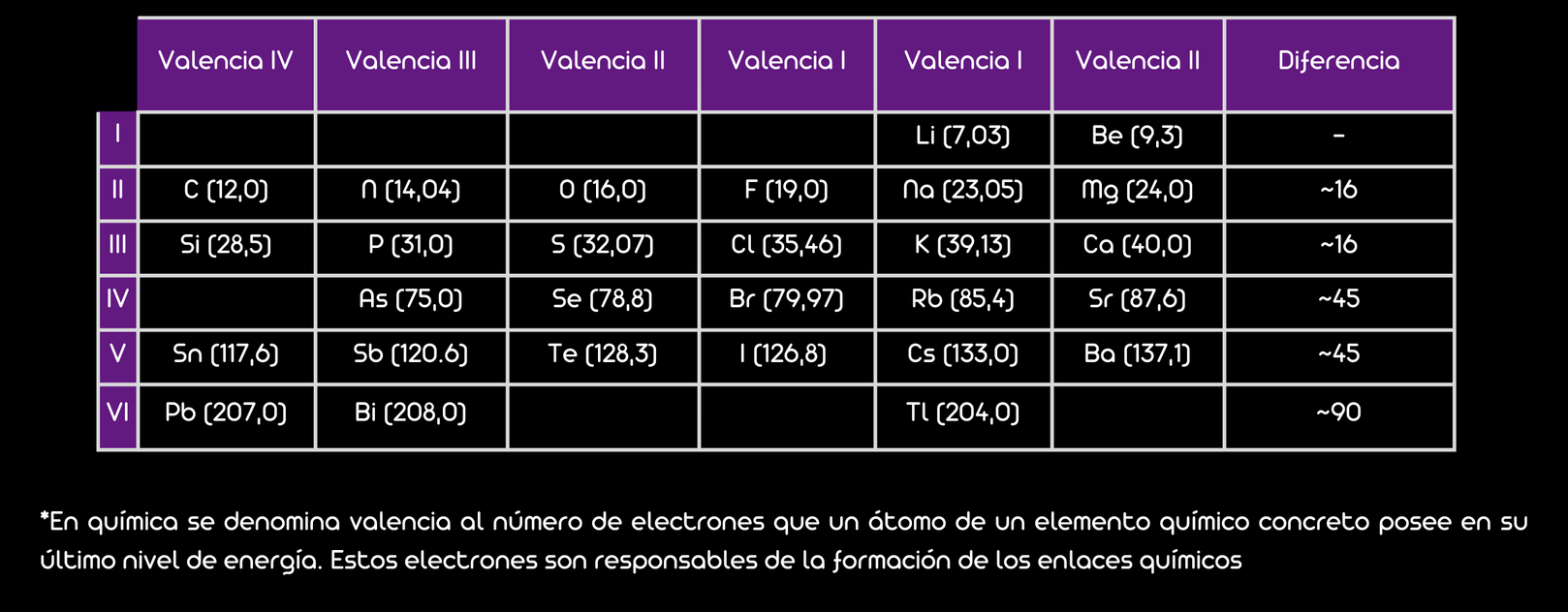
Por su parte, el químico alemán Julius Lothar Meyer (1830-1895) encontró otro tipo de correlaciones diferentes a las planteadas por Newlands. Esto lo llevó a formular su principal obra, el libro Teorías modernas de la química, empleando la hipótesis de Avogadro como punto de partida.

En el trabajo publicado se podían reconocer 28 elementos, con vacantes a la espera de su descubrimiento. Estos elementos fueron clasificados en seis familias en función de su valencia. Hasta entonces, los trabajos en el área se habían centrado en la organización por pesos equivalentes, en lugar de pesos atómicos.
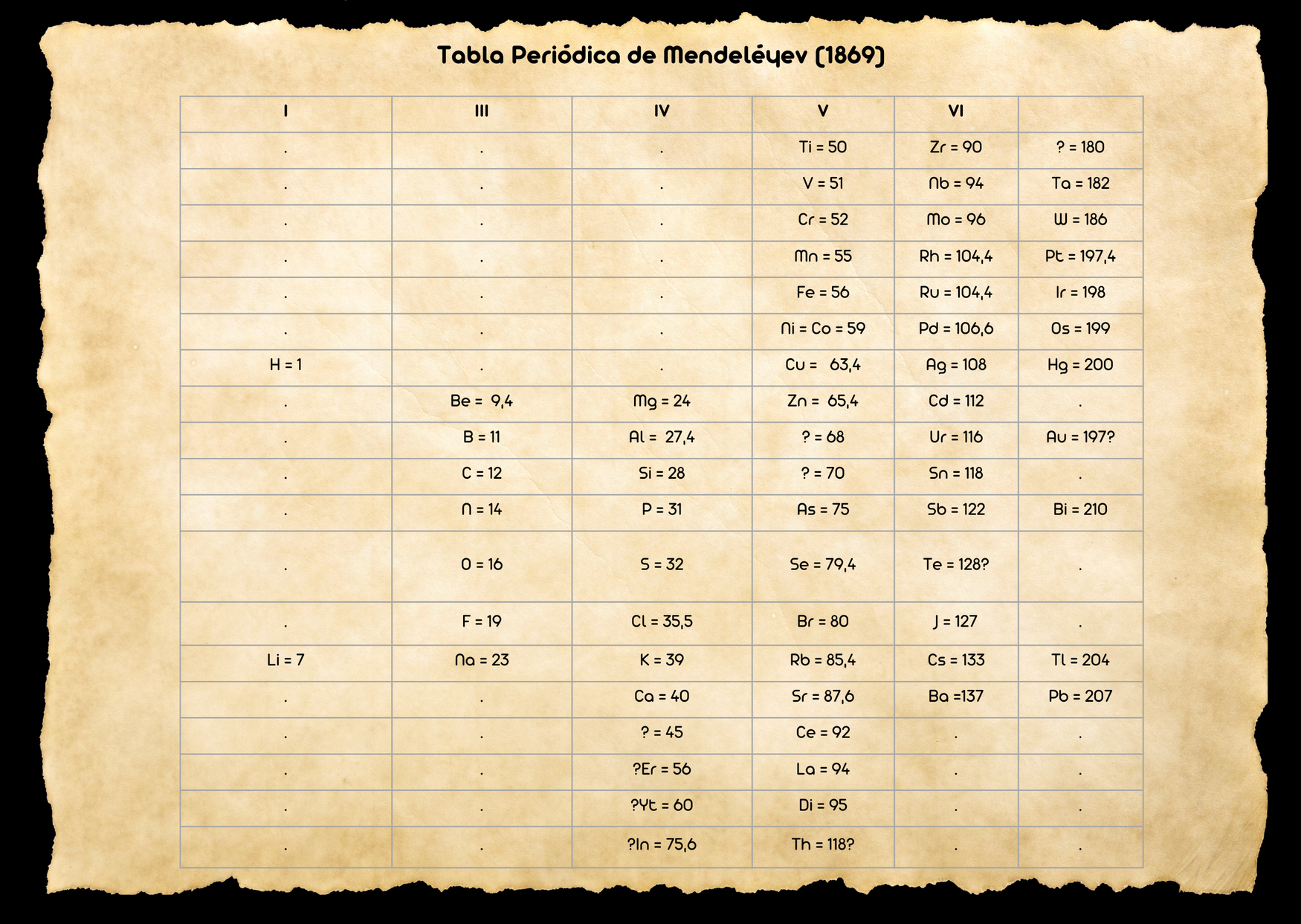
Año 1869: Tabla periódica de Mendeléyev
Los resultados de esta obra fueron complementados en 1869 por una nueva versión, pero el científico ruso Mendeleiev publicó simultáneamente un trabajo muy similar a la suya.

Mendeléyev organizó los elementos en orden creciente de sus masas atómicas, bajo la hipótesis de que las propiedades de los elementos guardan relación con sus pesos atómicos. Aunque inicialmente la tabla contaba con 60 elementos, supuso que faltaban elementos pendientes de descubrir y reservó huecos en la tabla, intuyendo las propiedades que podrían tener. Más tarde se añadieron a la tabla los gases nobles, pues en 1894 Ramsay y Rayleigh encontraron un gas monoatómico, químicamente inerte, que constituía algo menos del 1 por ciento de la composición atmosférica y al que denominaron argón. En 1898, Ramsay y Travers aislaron otros tres gases nobles denominados neón, criptón y xenón. En 1910, Ramsay demostró que el helio era el sexto gas noble, empleando para ello pequeñas muestras de radón.
Año 1896: Descubrimiento de la radioactividad
Podría decirse que uno de los grandes impulsores de esta tendencia en la bús-queda de la naturaleza nuclear del átomo fue el descubrimiento de la radiac-tividad. Hallazgos como el descubrimiento de los rayos X (1895) propiciaron que la comunidad científica orientaran su labor a la explicación de la naturaleza y producción de dichos fenómenos.
Así en 1896, Antoine Henri Becquerel descubre la radiactividad, investigando la posibilidad de producir radiaciones similares a los rayos X en sales de uranio que presentaban el fenómeno de la fluorescencia. Tras comprobar que en la más absoluta oscuridad estas seguían emitiendo radiación, concluye que no se trataba de una fluorescencia como la hasta entonces conocida, sino de otro fenómeno. Estas sales, que se encontraban sobre una placa fotográfica, y a pesar de estar en una zona oscura, oscurecían la placa. Esta investigación culmina con el descubrimiento de la radiactividad.

Un año más tarde (1897), Joseph John Thomson descubre la primera partícula subatómica, el electrón. Su investigación consistía en medir la relación entre la carga y la masa de los rayos catódicos, al medir cuánto se desvían por un campo magnético y la energía que llevan. De estos resultados dedujo que la relación carga/masa era más de mil veces superior a la del ion hidrógeno, dando a entender que dichas partículas eran muy livianas. Concluyó que estos rayos eran constituidos de partículas a las que denominó corpúsculos, y que estos corpúsculos venían de los átomos de los electrodos, dejando entrever que los átomos eran divisibles. Con esto, Thomson demostró que los rayos catódicos estaban compuestos por chorros de partículas minúsculas que no tardarían en identificarse como electrones, portadores de la carga eléctrica.
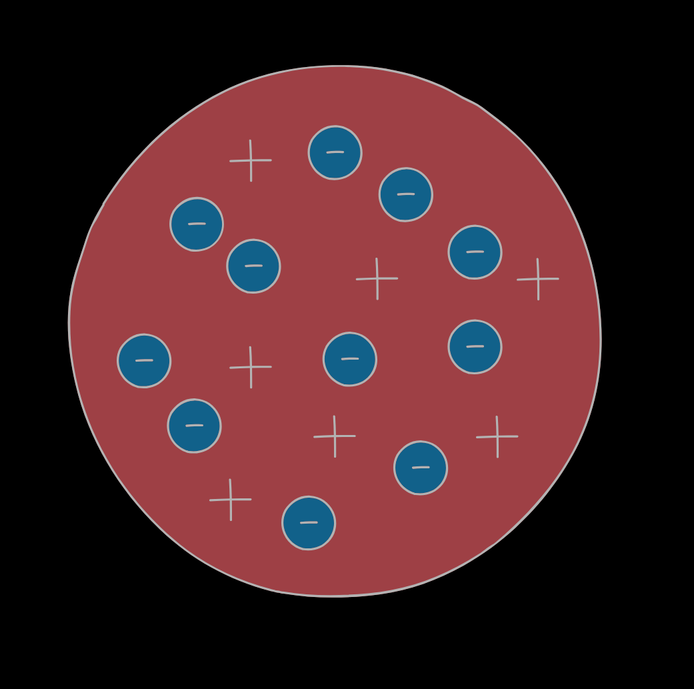
A la luz de estos descubrimientos, Thomson propone un modelo de átomo, que pasó a denominarse como <<modelo del pudín de pasas>>. En este modelo, los electrones (a los que él denominaba corpúsculos, y que vendrían a ser las pasas) estaban dispersos en una matriz con carga positiva que vendría a formar el pudín.
Año 1906: Modelo atómico de Thomson
En dicho modelo, y dado que Thomson había demostrado que el átomo más ligero (hidrógeno) tenía un peso de en torno a mil veces mas que el electrón, dedujo, erróneamente, que el átomo de hidrógeno tendría algo más de 1800 electrones, lo cual difiere bastante de la realidad, donde un átomo de hidrógeno contiene únicamente un electrón. Cabe destacar que aun no había sido descubierto ni el protón ni el neutrón, de ahí que al no haberse observado partículas positivas equivalentes, Thomson sugiriera este modelo donde la matriz positiva carecía de masa, y en consecuencia toda la masa fuera aportada por los electrones.

En 1906, Thomson, utilizando diferentes métodos para estimar el número de corpúsculos, llegó a la conclusión de que el número de estos no difiere mucho del peso atómico. Esta aproximación redujo el número de electrones de miles, o decenas de miles, a decenas, o centenares, y a su vez significó que la mayor parte de la masa del átomo recayera sobre la matriz positiva (pudín).
Modelo atómico del pudín de pasas

Año 1898: Descubrimiento del polonio y el radio
Influenciada por los descubrimientos recientes en radiactividad, Marie Curie decidió investigar los rayos de uranio para su tesis doctoral. Con la ayuda de su esposo, Pierre Curie, exploró la naturaleza de las radiaciones emitidas por las sales de uranio. Basándose en las notas de laboratorio de Lord Kelvin de finales de 1897, su objetivo inicial fue cuantificar la capacidad de ionización producida por estas sales. Para sus experimentos, Marie utilizó una técnica desarrollada quince años antes por Pierre y su hermano Jacques, quienes habían creado una versión mejorada del electrómetro. Con este dispositivo, Marie descubrió que los rayos de uranio permitían que el aire alrededor de una muestra se volviera conductor de electricidad. Utilizando esta técnica, determinó que la actividad radiactiva de los compuestos de uranio dependía únicamente de la cantidad de uranio presente. A partir de esto, propuso la hipótesis de que la radiación no era el resultado de interacciones moleculares, sino que provenía del propio átomo. Estas suposiciones fueron cruciales para desafiar la antigua creencia de que los átomos eran indivisibles, marcando un avance significativo en la comprensión de la estructura atómica.
En 1898, junto a su esposo Pierre Curie, descubrió dos elementos radiactivos: el polonio y el radio. El polonio, nombrado en honor a Polonia, la patria de Marie, y el radio, debido a su intensa radiactividad, fueron hallazgos cruciales que ampliaron el entendimiento de los elementos químicos y sus propiedades. Su trabajo se basó en los descubrimientos iniciales de Henri Becquerel sobre la radiactividad natural del uranio, pero los Curie lograron aislar y estudiar estos nuevos elementos en detalle, lo que les permitió comprender mejor la naturaleza de la radiactividad.

A pesar de que el torio fue identificado como elemento en 1828 por Berzelius, la radiactividad del torio fue observada por primera vez en 1898 por el químico alemán Gerhard Carl Schmidt y, de manera independiente, por Curie ese mismo año.

El aislamiento del radio en su forma pura por parte de Marie Curie fue un logro significativo que abrió nuevas vías de investigación y aplicaciones prácticas. Este avance permitió estudiar con mayor precisión las propiedades del radio, y su capacidad para emitir radiación fue fundamental para desarrollar la radioterapia, un tratamiento revolucionario para el cáncer que utiliza la radiación para destruir células malignas. Además, la radiactividad del radio se convirtió en una herramienta esencial para la investigación en física y química.
Las contribuciones de Marie Curie no se limitaron a sus descubrimientos científicos; también fundó el Instituto del Radio en París y en Varsovia, que se convirtieron en centros de investigación líderes en radiactividad y sus aplicaciones. Estos institutos han sido cruciales para el avance de la física nuclear y la medicina nuclear.


Año 1898: Modelo atómico de Rutherford
En 1898, Ernest Rutherford postula la existencia de dos clases de radiactividad, con distinto poder de penetración en la materia. Se denominaron radiación alfa (constituida por partículas alfa, o lo que es lo mismo, núcleos de helio), y radiación beta (electrones que se mueven a gran velocidad). Posteriormente, Paul Villard descubre la radiación con mayor poder de penetración, la radiación gamma (radiación electromagnética de mayor frecuencia).
En 1909 Rutherford junto con sus colaboradores Hans Geiger y Ernest Marsden, desarrollan en su laboratorio en Manchester, un experimento en el que dirigieron partículas alfa hacia una delgada lámina de oro. La mayoría de las partículas alfa atravesaron la lámina sin desviarse, pero algunas fueron desviadas en ángulos grandes, e incluso algunas rebotaron hacia la fuente. Dedujeron que los átomos de oro debían contener una carga positiva pequeña y concentrada que provocaba el rebote de las partículas alfa positivas. Estos resultados fueron sorprendentes y llevaron a Rutherford a proponer un nuevo modelo del átomo: en lugar de ser una masa uniforme de carga positiva con electrones incrustados (como sugería el modelo de Thomson), el átomo consistía en un núcleo denso y cargado positivamente en el centro, con los electrones orbitando alrededor de este núcleo. Rutherford también identificó al protón en 1918 y propuso la existencia del neutrón, descubrimiento que posteriormente fue confirmado por su estudiante James Chadwick en 1932.

Año 1900: Cuantización de la energía
A finales del siglo XIX, la física clásica se enfrentaba a un problema conocido como la "catástrofe ultravioleta". Según la teoría de la radiación de cuerpo negro basada en la física clásica, un objeto caliente debería emitir radiación de energía infinita a altas frecuencias, lo que claramente no se observaba en la realidad. Este dilema surgía de la aplicación de la ley de Rayleigh-Jeans, que predecía un aumento infinito de la radiación en el rango ultravioleta. Max Planck abordó este problema en 1900 proponiendo una solución radical que rompía con la física clásica: la teoría de la cuantización de la energía. Planck sugirió que la energía no se emite de manera continua, sino en pequeños paquetes discretos llamados "cuantos". Propuso que la energía de estos cuantos es proporcional a la frecuencia de la radiación, con la constante de proporcionalidad ahora conocida como la constante de Planck (ℎ).


Efecto fotoeléctrico
La teoría de Planck fue más tarde desarrollada por otros físicos, como Albert Einstein, quien utilizó el concepto de cuantos de luz para explicar el efecto fotoeléctrico, y Niels Bohr, quien aplicó la cuantización de la energía a su modelo del átomo de hidrógeno. En resumen, Max Planck resolvió el problema de la catástrofe ultravioleta proponiendo que la energía se emite en pequeños paquetes discretos, lo que llevó a la formulación de la constante de Planck y el nacimiento de la teoría cuántica, cambiando para siempre la comprensión de la física y la naturaleza de la radiación.
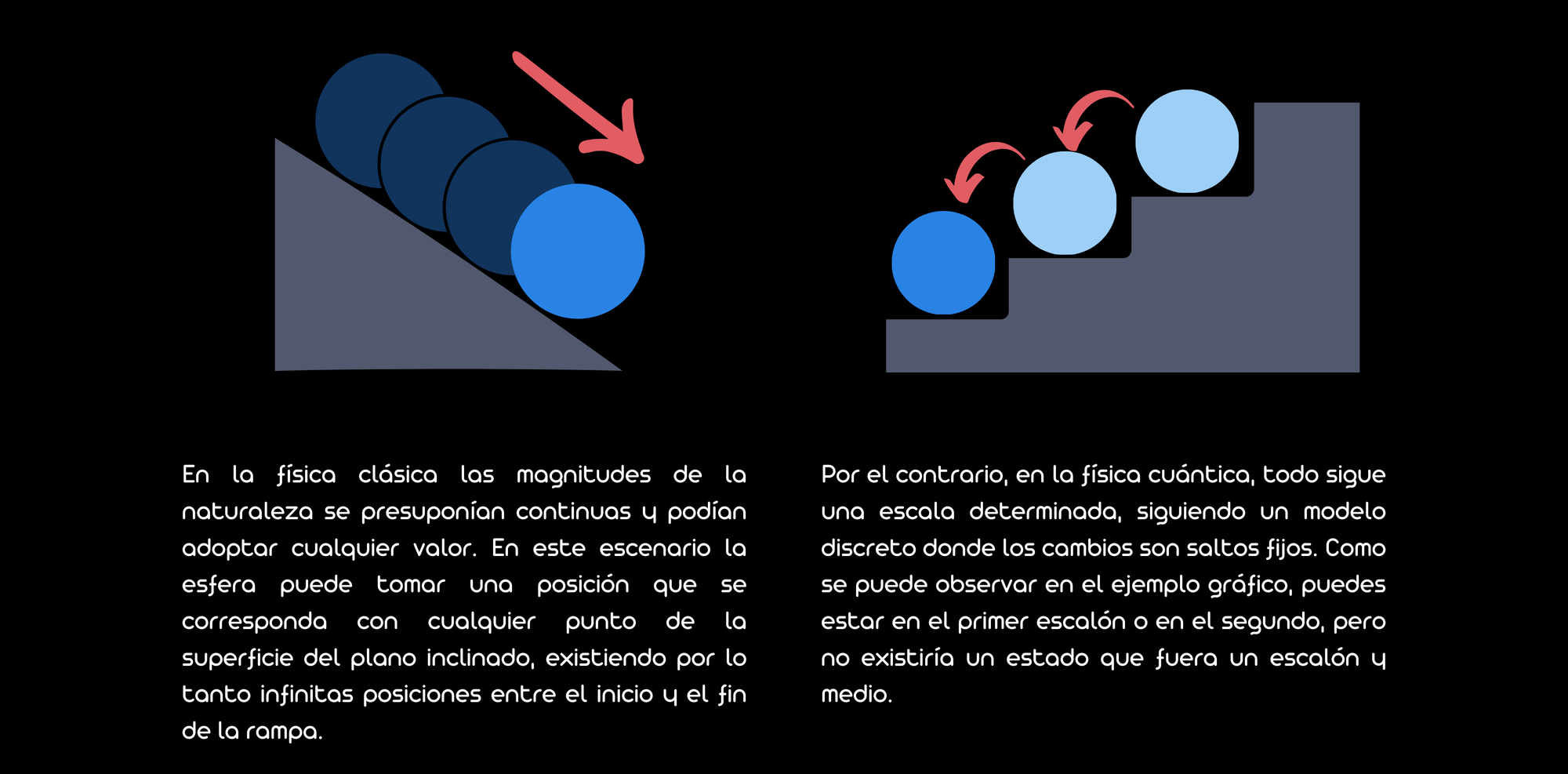
Planck, enfrentado a la discrepancia entre la teoría y los datos experimentales, recurrió a esta idea revolucionaria de la cuantización como un último recurso para obtener resultados coherentes. Según su propio relato, Planck afirmó que la introducción de los cuantos de energía fue una suposición puramente formal y que no le dedicó mucho pensamiento, sino que lo hizo a cualquier costo para lograr un resultado positivo.
Poco tiempo después, Einstein se aventuró a plantear que la luz estaba compuesta de paquetes de partículas, que posteriormente se denominarían como fotones. Para ello se apoyó en las observaciones de Lenard; pues desde la década de 1880 se vio que al dirigir luz intensa sobre determinados metales, saltaban electrones. En estos primeros experimentos se irradió con luz ultravioleta de alta frecuencia, deduciendo que a mayor intensidad, mayor cantidad de electricidad se producía. Hasta aquí todo casaba con los modelos existentes, basados en la teoría de Maxwell, que daban por sentado que la luz era una onda electromagnética.
El problema vino cuando Lenard observa que el color de la luz determinaba el resultado. Se determinó que si la frecuencia de la luz era demasiado baja, es decir, hacia el extremo rojo del espectro, no se producía ningún efecto, con independencia de la intensidad de la luz. Por el contrario, un haz de luz azul de baja intensidad si producía electricidad.

Año 1905: Movimiento browniano
Por otro lado, la teoría de Einstein sobre el movimiento browniano, publicada en 1905, fue una de sus contribuciones más significativas junto con el efecto fotoeléctrico y la relatividad, y proporcionó una evidencia contundente para la existencia de los átomos y moléculas, reforzando así los modelos atómicos de la materia. El movimiento browniano se refiere al movimiento errático y aleatorio de partículas microscópicas suspendidas en un fluido (líquido o gas), observado por primera vez por el botánico Robert Brown en 1827. Aunque Brown no pudo explicar este fenómeno, Einstein propuso una teoría que lo hacía comprensible en términos de la teoría cinética de los gases, sugiriendo que las partículas suspendidas están siendo constantemente golpeadas por las moléculas del fluido en el que están inmersas. Estas colisiones moleculares, aunque invisibles, producen un movimiento observable de las partículas suspendidas.

Einstein desarrolló una fórmula que relaciona la magnitud del desplazamiento de las partículas con la temperatura del fluido y la viscosidad del fluido, junto con el tamaño de las partículas. Esto confirmaba la hipótesis de que el agua estaba compuesta de moléculas diminutas, pues aunque esta teoría no profundizó sobre la naturaleza de los átomos, los resultados se tomaron como una prueba de que la teoría atómica no sólo era un modelo útil.
Rastros del movimiento de partículas coloidales

Jean Baptiste Perrin fue quien corroboró experimentalmente la teoría del movimiento browniano propuesta por Albert Einstein. A partir de 1908, Perrin llevó a cabo una serie de experimentos meticulosos que verificaron las predicciones teóricas de Einstein sobre el movimiento browniano, proporcionando así una prueba sólida de la existencia de átomos y moléculas. Para ello, Perrin estudió el comportamiento de partículas suspendidas en un líquido bajo el microscopio, midiendo sus movimientos y confirmando que coincidían con las predicciones de Einstein sobre la distribución y el movimiento de partículas debido a las colisiones con las moléculas del líquido. Estos experimentos permitieron determinar valores precisos para la constante de Avogadro y proporcionaron una evidencia irrefutable de la teoría atómica. Por su trabajo, Jean Baptiste Perrin recibió el Premio Nobel de Física en 1926. Sus investigaciones no solo validaron la teoría de Einstein, sino que también pusieron fin a un largo debate sobre la realidad física de los átomos y moléculas, estableciendo firmemente la teoría atómica en la ciencia moderna.
Año 1905: Ecuación masa-energía
También por parte de Einstein, y formulada en 1905 en la teoría de la relatividad especial, se introdujo la famosa ecuación que relacionaba masa y energía:
E=mc2
donde E sería la energía, m la masa, y c la velocidad de la luz (aproximadamente 300.000.000 m/s)
Aunque cuando desarrolló la teoría de la relatividad especial no estaba pensando en las aplicaciones a la física nuclear, ya que su principal objetivo era resolver otros problemas fundamentales de la física teórica, esta célebre ecuación, que mostraba que la masa y la energía podían ser intercambiables, abrió posteriormente otras vías de desarrollo. La idea de que pequeñas cantidades de masa pueden ser convertidas en grandes cantidades de energía se convirtió en la base para comprender las reacciones nucleares y condujo al desarrollo de la bomba atómica y la energía nuclear.

Año 1913: Descubrimiento de los isótopos
Entre 1902 y 1903, se desarrolló una teoría propuesta por Soddy junto con Rutherford que explicaba cómo los elementos radiactivos se transforman espontáneamente en otros elementos a través de la emisión de partículas alfa, beta y gamma. Este proceso de desintegración radiactiva cambia la identidad del elemento, y pasó a convertirse en una pieza clave en la comprensión de la radiactividad y la transmutación de los elementos.
Una década más tarde, en 1913, Soddy acuñó el término "isótopo" (del griego "isos" que significa "igual" y "topos" que significa "lugar") para describir estos átomos que ocupan el mismo lugar en la tabla periódica pero tienen diferentes masas atómicas. Observó que ciertos elementos radiactivos, como el torio y el uranio, emitían partículas que llevaban a la formación de otros elementos con las mismas propiedades químicas pero con diferentes masas atómicas. Este descubrimiento fue crucial para la química y la física, ya que explicó por qué ciertos elementos presentaban comportamientos químicos idénticos a pesar de tener diferentes masas.






