El modelo atómico. Parte II: del modelo atómico de Bohr al modelo estándar

En la primera parte de esta serie vimos cómo el modelo atómico fue tomando forma desde las primeras ideas filosóficas sobre el átomo hasta la propuesta nuclear de Rutherford. Aquel recorrido permitió entender cómo el átomo dejó de ser una noción abstracta para convertirse en un objeto de estudio físico cada vez más definido.

Sin embargo, el modelo de Rutherford, pese a su carácter revolucionario, dejaba abiertas preguntas esenciales. Si el átomo concentraba casi toda su masa en un núcleo diminuto y los electrones orbitaban a su alrededor, ¿qué impedía que esos electrones perdieran energía y colapsaran sobre el núcleo? ¿Y cómo explicar, además, que los átomos emitieran y absorbieran luz de manera discreta, siguiendo patrones bien definidos? Estas limitaciones hicieron evidente que hacía falta un nuevo marco teórico. Ese siguiente paso llegaría con el modelo de Bohr, que introdujo la cuantización en la estructura atómica y abrió la puerta a una comprensión más profunda del átomo, al tiempo que el avance experimental seguía revelando que su interior era mucho más rico y complejo de lo que se había imaginado, con el descubrimiento progresivo de nuevas partículas fundamentales.
Año 1913: Modelo atómico de Bohr
En 1913, Bohr, usando como punto de partida el modelo de núcleo positivo pesado rodeado de electrones propuesto por Rutherford, y basándose en las teorías de cuantización de Planck y Einstein, propuso que el propio electrón estaba cuantizado. Esto implicaba que el electrón no podía existir en cualquier lugar del átomo, como si sugería el modelo de Rutherford. En este modelo el electrón sólo podía encontrarse en posiciones específicas, con energías específicas. El electrón tenía posibilidad de “saltar” entre posiciones pero sólo en pasos discretos y definidos, limitándose por tanto a regiones concretas del espacio, de una forma similar a como lo hacen los planetas en el sistema solar. La energía absorbida o emitida en estos saltos corresponde a la diferencia de energía entre los niveles y se manifiesta en forma de radiación electromagnética, lo cual explica las líneas espectrales observadas en la emisión de átomos.

Año 1913: Ley de Moseley
En el mismo año en el que Bohr propone su modelo atómico (1913), Moseley anuncia la ley que lleva su nombre. Realizando una serie de experimentos utilizando rayos X para estudiar los elementos, llegó al descubrimiento de que la frecuencia de los rayos X emitidos por los átomos de diferentes elementos se correlacionaba con su número atómico, no con su peso atómico, como se pensaba anteriormente. Este descubrimiento permitió reorganizar la tabla periódica de los elementos según su número atómico, resolviendo inconsistencias previas y prediciendo la existencia de elementos aún no descubiertos. Esta correlación se conoce hoy como la Ley de Moseley.

Año 1916: Estructura de Lewis
En 1916, Lewis propuso la teoría del enlace covalente, sugiriendo que los átomos comparten electrones para alcanzar configuraciones electrónicas estables, similares a las de los gases nobles. Esta teoría se basa en el concepto de la "regla del octeto", que establece que los átomos tienden a completar su capa de valencia con ocho electrones.
El modelo del átomo cúbico, propuesto por Lewis en 1916, describe los átomos como cubos con electrones en sus vértices. Aunque pronto fue reemplazado por el modelo mecánico cuántico basado en la ecuación de Schrödinger, este modelo representó un avance importante en la comprensión del enlace químico, al introducir la idea de que los átomos comparten electrones para alcanzar configuraciones estables.

Lewis también introdujo el diagrama de puntos de Lewis, también denominado estructura de Lewis, una representación visual que muestra los electrones de valencia de un átomo y cómo estos se comparten o transfieren para formar enlaces químicos. Esta herramienta gráfica simplificó la comprensión y predicción de la estructura molecular. Además, Lewis contribuyó a la comprensión de los ácidos y bases mediante su definición, que describe un ácido como un receptor de pares de electrones y una base como un donador de pares de electrones.

Modelo atómico de Sommerfeld
También en 1916 Arnold Sommerfeld extiende el modelo atómico de Bohr introduciendo órbitas elípticas además de las circulares. Esto permitió dar una mejor explicación de los espectros atómicos de elementos con más de un electrón.
Aun cuando el modelo atómico de Bohr funcionaba bien para el átomo de hidrógeno, presentaba algunos problemas con los espectros de otros elementos. Se observó que los electrones con el mismo nivel energético tenían energías diferentes, lo que indicaba un error en el modelo. La conclusión fue que dentro de un mismo nivel energético existían subniveles, con energías ligeramente distintas. Además, Sommerfeld encontró que en ciertos átomos las velocidades de los electrones alcanzaban una fracción significativa de la velocidad de la luz. Este nuevo modelo propuesto de órbitas elípticas alrededor del núcleo lleva a la cuantización de la excentricidad de estas órbitas, y es una generalización del modelo atómico de Bohr desde un punto de vista relativista.

Año 1924: Dualidad onda-partícula
A lo largo del siglo XIX, numerosos experimentos, como los realizados por Thomas Young, demostraron que la luz se comporta como onda. Maxwell, en su teoría de la electricidad y el magnetismo, consolida esta idea, al describir la luz como una onda electromagnética. En 1905, Albert Einstein explicó el efecto fotoeléctrico, proponiendo la idea de que la luz está compuesta por partículas llamadas fotones, cada una con una energía discreta proporcional a su frecuencia, demostrando con ello la naturaleza corpuscular de la luz.
Ahora bien, ¿qué es realmente la luz?
¿Onda o partícula?
¿Ambas cosas o ninguna?
En 1924, De Broglie propuso que no solo la luz, sino todas las partículas de materia, tienen propiedades de onda. Esta idea revolucionaria surgió de su tesis doctoral, donde postuló que las partículas como los electrones podrían comportarse como ondas bajo ciertas condiciones. Esto significa que una partícula puede tener una longitud de onda asociada, ahora conocida como la longitud de onda de de Broglie, que está inversamente relacionada con su momento. Su hipótesis proporcionó una nueva perspectiva sobre la naturaleza de la materia, sugiriendo que los fenómenos cuánticos deben considerarse en términos tanto de partículas como de ondas.
La propuesta de De Broglie fue confirmada experimentalmente por los experimentos de difracción de electrones realizados por Clinton Davisson y Lester Germer en 1927. Estos experimentos demostraron que los electrones pueden mostrar patrones de interferencia típicos de las ondas, validando la hipótesis de De Broglie. Esto llevó al desarrollo de la mecánica ondulatoria por Erwin Schrödinger, quien utilizó el concepto de ondas de materia para formular su famosa ecuación de onda, que describe cómo las ondas de materia evolucionan en el tiempo.


“Toda la materia presenta características tanto ondulatorias como corpusculares comportándose de uno u otro modo dependiendo del experimento específico.”
Louis de Broglie
Año 1925: Mecánica matricial
Con una visión alejada de los modelos hasta el momento propuestos, por estar demasiado anclados en el “mundo clásico”, Heisenberg desarrolló junto con Born y Jordan un modelo matemático de las partículas cuánticas denominado mecánica cuántica matricial. No era un modelo en el sentido estricto al que estamos acostumbrados, a modo de diagrama visual, sino una descripción matemática del comportamiento de los electrones y otras partículas subatómicas. En este nuevo modelo, en lugar de describir las órbitas de los electrones alrededor del núcleo como en los modelos de Bohr y Sommerfeld, la mecánica matricial utiliza matrices para describir los estados cuánticos de las partículas. Estos estados no son posiciones y velocidades definidas, sino probabilidades de encontrar partículas en ciertos estados.

La mecánica matricial fue la primera implementación matemática completa de la mecánica cuántica, sin embargo, cae rápidamente en el olvido tras la aparición de la formulación de la mecánica ondulatoria de Schrödinger.
Heisenberg y Bohr en 1934. Crédito: Fermilab, U.S. Department of Energy

Año 1926: Mecánica ondulatoria
El modelo ondulatorio del átomo de Schrödinger, también conocido como la mecánica ondulatoria, es una descripción de la estructura atómica que se basa en la idea de que los electrones exhiben propiedades tanto de partículas como de ondas. En 1926, Erwin Schrödinger desarrolló una ecuación de onda que describe cómo el estado cuántico de un sistema físico cambia con el tiempo.

Año 1928: Ecuación de Dirac
En 1928, Paul Dirac formuló la ecuación de Dirac, una extensión de la ecuación de Schrödinger que incorpora los efectos relativistas. Esta ecuación describe el comportamiento de los electrones y otras partículas de espín 1/2, y predice la existencia de antipartículas.

Año 1932: Descubrimiento del neutrón
Hasta la fecha se desconocía la causa por la cual cabía la posibilidad de que hubiera versiones distintas de un mismo elemento, con masas diferentes, y que contaban con las mismas propiedades químicas esperadas. Pese a que la solución de suponer que el núcleo contenía partículas neutras ya fue propuesta en 1920 por Rutherford, los intentos de plantearlos como pares protón-electrón fracasaron.
Fue en 1932 cuando james Chadwick descubrió la existencia del neutrón, que se mostraba como una partícula sin carga eléctrica, con una masa similar a la del protón y con entidad propia, en el sentido de que eran partículas independientes. Para ello, partió de los experimentos de Frédéric e Irène Joliot-Curie, que bombardearon berilio con partículas alfa, produciendo en el proceso una radiación altamente penetrante que no podía ser explicada por los rayos gamma. Chadwick estaba al tanto de estos resultados y sospechaba que esta radiación podría ser una nueva partícula neutra. Repitió y extendió los experimentos; y bombardeó berilio con partículas alfa procedentes de una fuente de polonio. La radiación emitida por el berilio golpeó una muestra de parafina, un material rico en protones (núcleos de hidrógeno). Procedió a medir los protones que fueron expulsados de la parafina y observó que los protones eran emitidos con una energía que no podía ser explicada por la interacción con los rayos gamma.
Experimento llevado a cabo por Chadwick
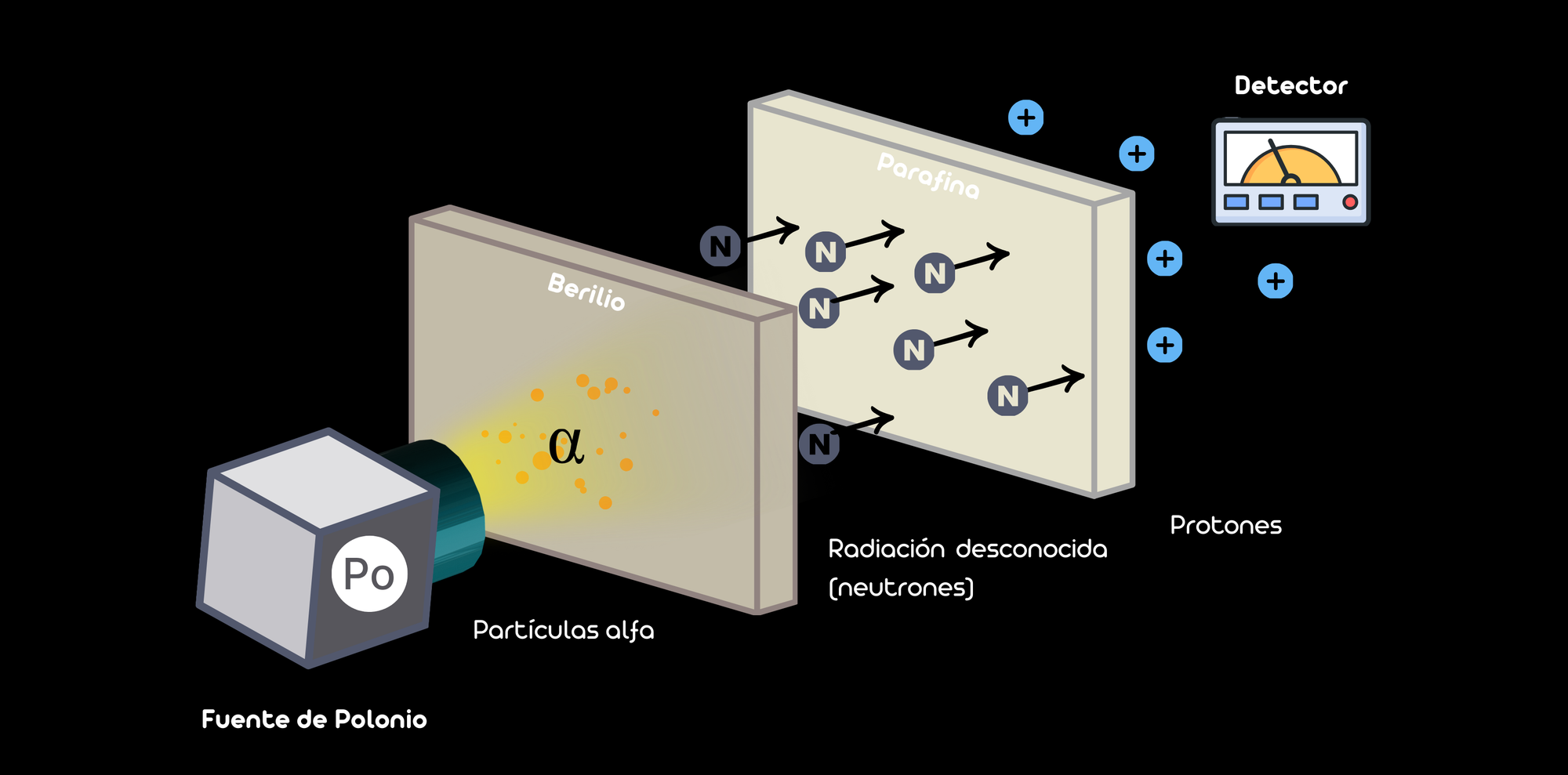
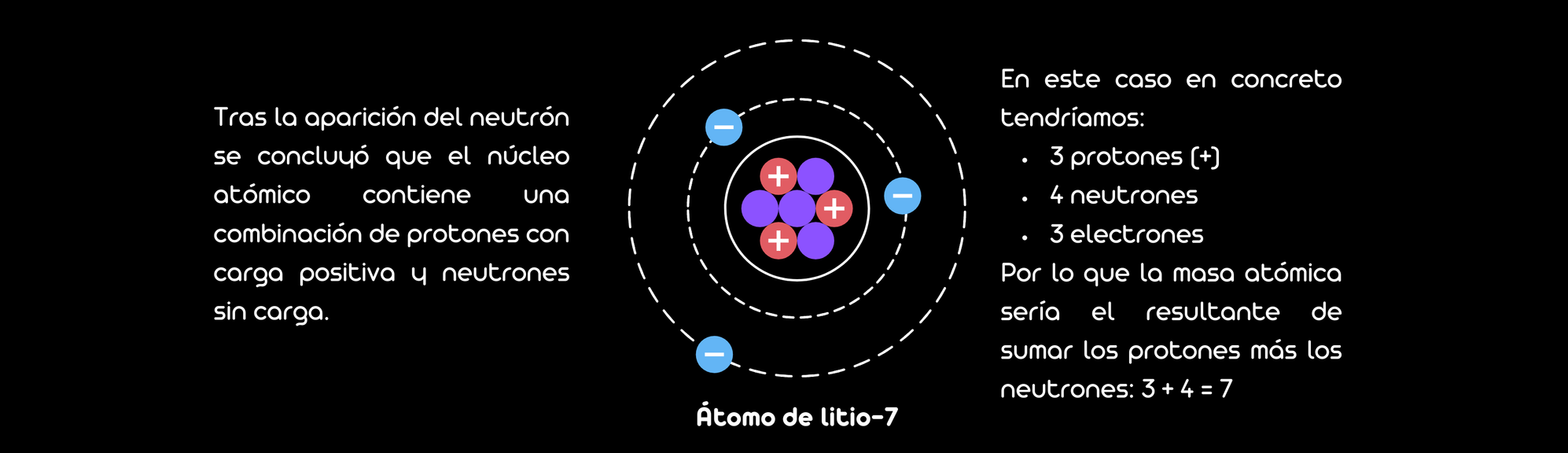
A partir de la energía de los protones expulsados y utilizando principios de conservación de energía y momento, Chadwick concluyó que la radiación debía consistir en partículas de masa similar a la del protón pero sin carga eléctrica. Calculó la masa de esta nueva partícula y encontró que era aproximadamente igual a la del protón, de donde concluyó que la nueva partícula era el neutrón.
Este hallazgo fue crucial porque resolvió el problema de la masa atómica que no podía ser explicado solo con protones y electrones. Los neutrones completaron el modelo del núcleo atómico, permitiendo una comprensión más profunda de la estructura atómica y dieron una explicación a la variedad de pesos atómicos de los isótopos. Por su descubrimiento del neutrón, Chadwick recibió el Premio Nobel de Física en 1935.
Además, su trabajo fue fundamental para el desarrollo de la energía nuclear, tanto en aplicaciones pacíficas como en la creación de armas nucleares. Durante la Segunda Guerra Mundial, Chadwick fue una figura clave en el Proyecto Manhattan, que desarrolló la primera bomba atómica. Su liderazgo en el proyecto y su conocimiento en física nuclear fueron esenciales para el éxito.

Año 1932: Descubrimiento del positrón
Si bien el positrón (antipartícula del electrón) fue predicho teóricamente por Paul Dirac en 1928, no fue hasta 1932 cuando Carl David Anderson lo descubrió mientras estudiaba los rayos cósmicos utilizando una cámara de niebla en el Instituto de Tecnología de California (Caltech). Tras analizar una traza en la cámara de niebla que se curvaba en una dirección opuesta a la que se esperaba para un electrón en presencia de un campo magnético, concluyó que tenía una masa similar al electrón pero con una carga positiva.

Año 1938: Descubrimiento de la fisión nuclear
Inspirado por el descubrimiento del neutrón por James Chadwick en 1932, Fermi reconoció que los neutrones, al carecer de carga eléctrica, podrían ser usados para penetrar fácilmente en los núcleos atómicos. A diferencia de las partículas alfa o protones, los neutrones no eran repelidos por la carga positiva del núcleo, lo que les permitía acercarse y ser absorbidos por el núcleo atómico más fácilmente. En 1934, Fermi comenzó a realizar experimentos en los que bombardeaba diversos elementos con neutrones. Descubrió que, al absorber un neutrón, muchos elementos se volvían radiactivos, transformándose en isótopos diferentes que no existían de manera natural. Uno de los descubrimientos más importantes en este contexto fue que los neutrones "lentos" (aquellos con energía baja) eran más efectivos en inducir la radiactividad que los neutrones "rápidos". Fermi y su equipo descubrieron que al pasar los neutrones a través de una sustancia moderadora, como la parafina o el agua, su velocidad se reducía, lo que aumentaba la probabilidad de que fueran capturados por los núcleos atómicos. Por sus hallazgos sobre la existencia de nuevos elementos radiactivos derivados de la irradiación con neutrones, Fermi fue galardonado en 1938 con el premio Nobel de Física.

Aunque Fermi no consiguió la fisión nuclear en sus experimentos, sus investigaciones con neutrones sentaron las bases para el descubrimiento en diciembre de 1938 de la fisión nuclear, por parte de Otto Hahn y Fritz Strassmann. En estos experimentos se logró dividir el núcleo de uranio, produciendo elementos mucho más ligeros, pero no pudieron explicar del todo los resultados. Al año siguiente Lise Meitner, que ya había colaborado previamente con Hahn, y junto con la colaboración de Otto Frisch, proporcionó la interpretación teórica de los resultados.


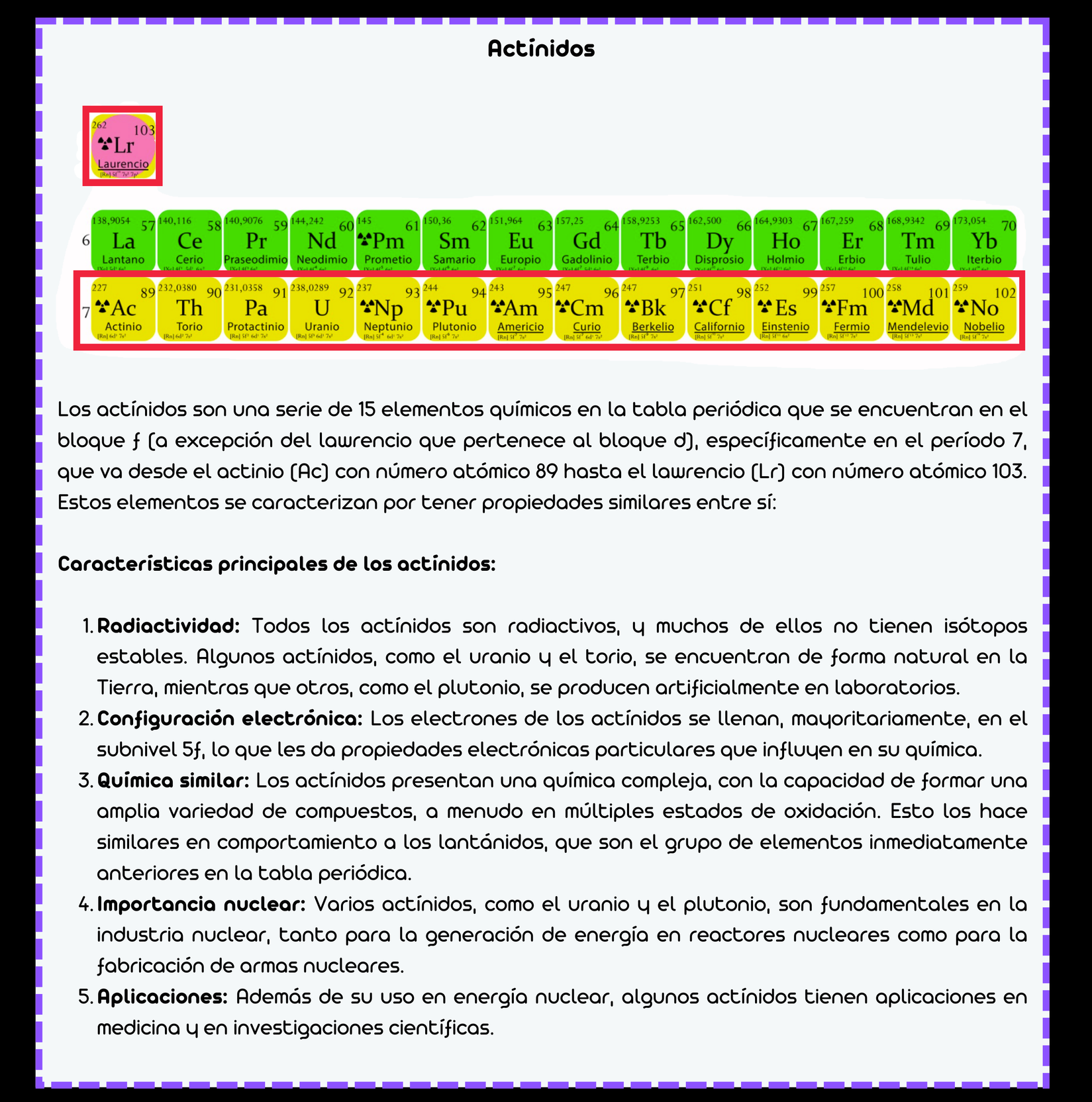
1940-1958: Actínidos
Aunque la existencia de elementos transuránicos (más allá del uranio en la tabla periódica) fue sugerida por Enrico Fermi en 1934, tuvieron que pasar unos años para que estos elementos fueran aislados e identificados. Entre 1940 y 1958 se identificaron varios elementos transuránicos. Uno de los codescubridores más célebres fue Glenn T. Seaborg. Estos elementos incluyen el plutonio, americio, curio, berkelio, californio, einstenio, fermio, mendelevio, nobelio y el seaborgio, que fue nombrado en su honor. De entre todos ellos, el descubrimiento del plutonio fue particularmente significativo, ya que se convirtió en un componente clave en el desarrollo de armas nucleares y reactores nucleares durante y después de la Segunda Guerra Mundial.
Seaborg propuso una reorganización de la tabla periódica en 1945, desarrollando el concepto de elementos actínidos, y sugiriendo que dichos elementos (similares a los lantánidos) deberían formar una serie separada, conocida como la serie de los actínidos. Seaborg recibió el Premio Nobel de Química junto con Edwin McMillan por sus descubrimientos en la química de los elementos transuránicos.
Descubrimiento de partículas fundamentales
Tras el descubrimiento del neutrón y el positrón en 1932, y la teorización de otras partículas como el fotón (1905) o el neutrino (1930), se tenía una idea más o menos establecida de lo que se creía que eran las partículas fundamentales. Lejos de esto, en los años venideros, y con el concurso de los colisionadores de partículas, surgieron una variedad de nuevas partículas. A las partículas ya existentes se sumó el muón en 1936, descubierto por Carl D. Anderson y Seth Neddermeyer durante estudios de la radiación cósmica; y confirmada su existencia por parte de J.C. Street y E.C. Stevenson. Fue la primera partícula fundamental descubierta que no pertenecía a los átomos convencionales y en cuestión de unos pocos años, la imagen de ese universo formado por unas cuantas partículas elementales se vino abajo, en aras de un universo constituido por multitud de partículas diversas, lo que indujo la aparición de nuevas teorías que dieran cabida a este “mundo” aun por descubrir.
En 1947 se incluiría al pión, ya teorizado por Hideki Yukawa en 1935. Fue descubierto por Cecil Powell, César Lattes y Giuseppe Occhialini, tras exponer placas fotográficas a radiación cósmica. En ese mismo año, George Rochester y Clifford Butler descubren los kaones, también en estudios de radiación cósmica. Tanto el pión como el kaón fueron posteriormente identificados como mesones. Durante estos años se identificaron otros mesones, como los omega, J, eta, úpsilon, entre otros.
En 1962, aunque teorizado en la década de 1940, se descubre el neutrino muónico por parte de Leon M. Lederman, Melvin Schawartz y Jack Steinberger. También en esa misma década se teorizan los quarks up, down y strange, siendo confirmados experimentalmente en la década siguiente mediante técnicas de dispersión profunda inelástica. A estos se sumarian los quarks charm (c) en 1974, y el bottom (b) en 1977.
Predicho por la cromodinámica cuántica propuesta por Murray Gell-Mann a inicios de los setenta, en 1979 se identifica al gluón mediante experimentos de colisiones de alta energía. Unos años más tarde, y teorizados en los sesenta por la teoría electrodébil, son descubiertos los bosones W y Z (1983), por Carlos Rubbia en colaboración con el equipo del CERN.
En 1995, tras su especulación debido al descubrimiento del quark bottom, es descubierto en el Fermilab el quark top (t) mediante colisiones de alta energía en el Tevatrón, culminando con el descubrimiento de los seis quarks predichos.
Por el momento, la última partícula descubierta es el bosón de Higgs, teorizado por Peter Higgs, François Englert, Robert Brout y otros colaboradores en 1964. En 2012 fue descubierto el bosón de Higgs en el Gran Colisionador de Hadrones (LHC), confirmando el mecanismo de Higgs, que otorga masa a las partículas fundamentales.
A modo de síntesis se muestra un resumen de la evolución que ha sufrido el modelo atómico hasta llegar a su representación actual.

El Modelo Estándar
Basado en la mecánica cuántica, y como evolución de los modelos atómicos de Rutherford, Bohr y Sommerfeld, no cabe lugar al concepto de órbitas electrónicas de tipo planetarios, aunque dicho sistema puede servir a modo didáctico para explicar diferentes conceptos. En el modelo actual, el electrón a escala atómica se comporta fundamentalmente como una onda, mientras que a una escala más macroscópica su comportamiento es corpuscular. Su comportamiento viene dado por los siguientes principios ya expuestos:
- Dualidad onda-partícula
- Principio de incertidumbre de Heisenberg
- Ecuación de Schrödinger
En lo que respecta a sus características:
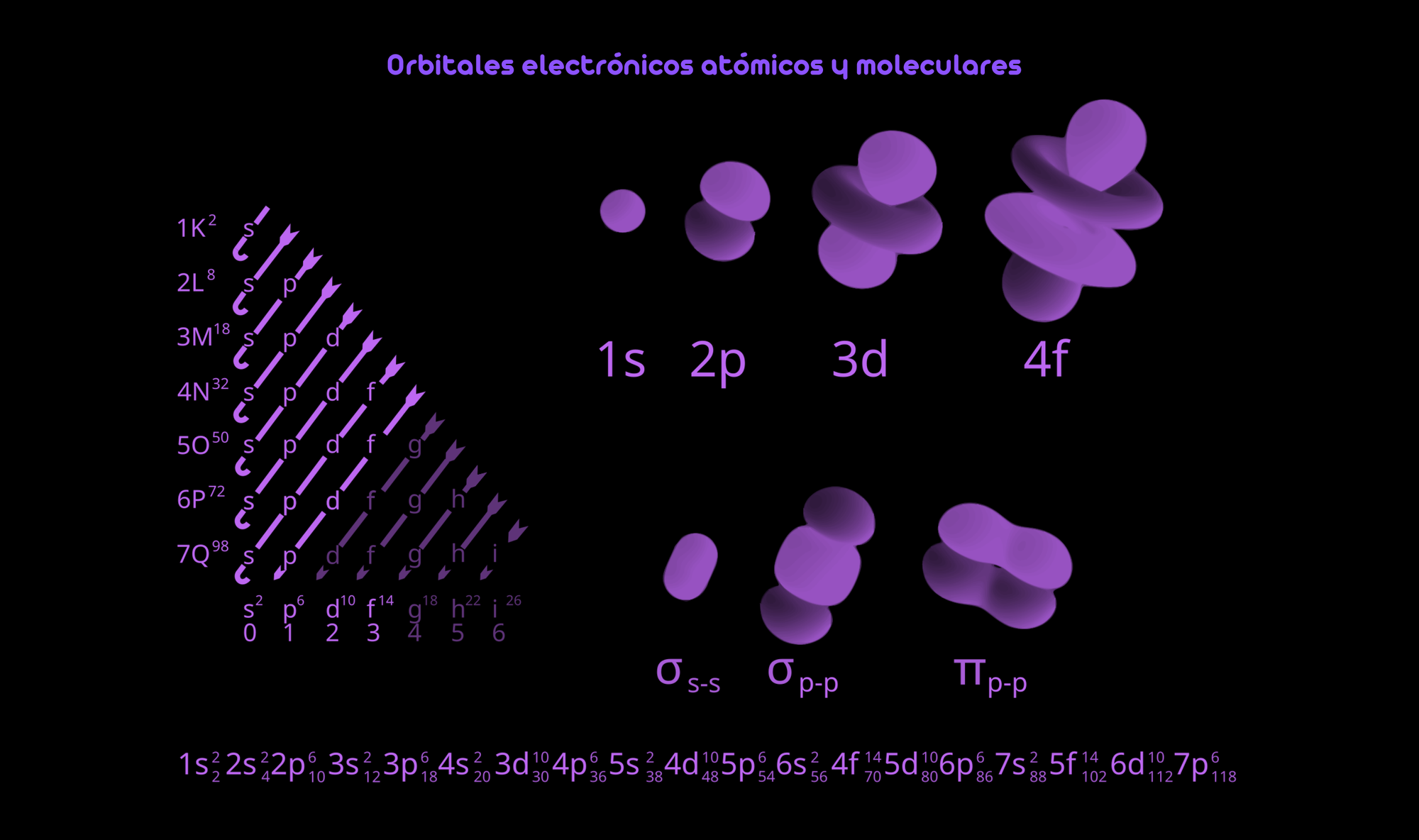
- Los electrones no siguen trayectorias fijas, sino que existen regiones denominadas orbitales donde existe una probabilidad de encontrar un electrón. Estos orbitales tienen diferentes formas, que pueden ser esféricas, lobulares o de otro tipo. Los orbitales se designan como s, p, d y f, y están organizados en capas y subcapas, como 1s, 2s, 2p, 3s, etc.
- Los electrones sólo pueden establecerse en ciertos niveles energéticos, como consecuencia de la cuantización de la energía. Por lo que cuando absorbe o emite energía se mueve entre niveles discretos.
- La configuración electrónica que define la disposición de los electrones está regida por los principios de exclusión de Pauli, por lo que cada orbital puede tener como máximo dos electrones con espines opuestos. Además, el principio de Aufbau impone que los electrones se ubican en primer lugar en los orbitales menos energéticos.
- Puesto que se aplica el principio de incertidumbre dada la naturaleza cuántica de los electrones, no se puede determinar con precisión su posición y su velocidad simultáneamente.
Tal y como se ha indicado previamente, en línea con la mecánica ondulatoria, el movimiento de una partícula en un campo de fuerzas se puede obtener a través de la ecuación de Schrödinger:

Para un sistema unidimensional el operador momento se reemplaza según:
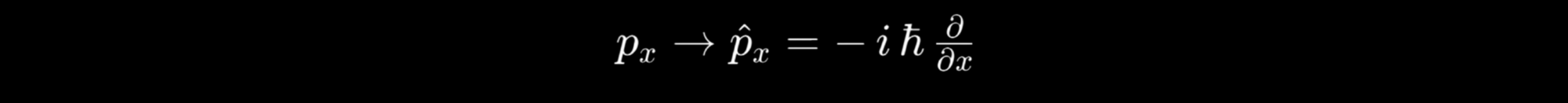
generalizado en tres dimensiones como
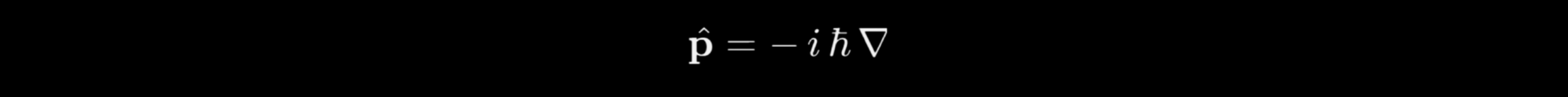
Cuando el potencial V(r) no depende explícitamente del tiempo se puede hacer la separación de variables de la función de onda:
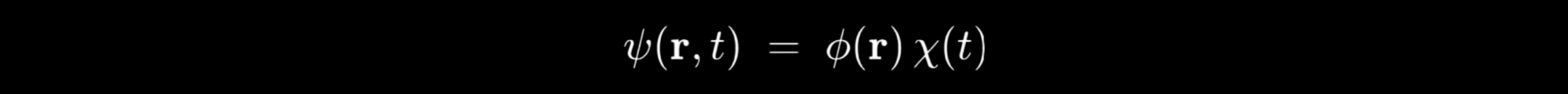
Al introducir esto en la ecuación original se obtiene la ecuación de Schrödinger independiente del tiempo para la parte espacial ϕ(r):
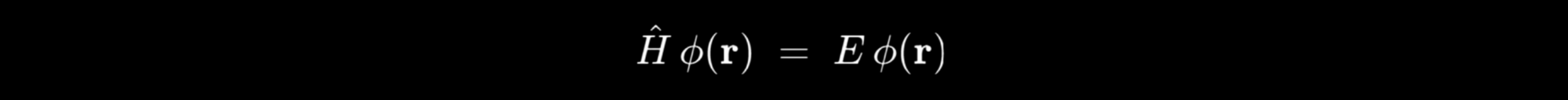
donde E es la energía (el valor propio asociado al estado cuántico)
- Las soluciones de la ecuación se denominan funciones propias, con valores propios de energía.
- Estos valores de energía pueden ser discretos (estados ligados) o continuos (estados de dispersión), dependiendo del tipo de pozo de potencial o de la interacción coulombiana en el átomo.
- En el caso del átomo de hidrógeno, los estados ligados se caracterizan por los números cuánticos:
- n (principal), relacionado con el número total de nodos en la función propia.
- l (azimutal), relacionado con el momento angular.
- m (magnético), que especifica la orientación del momento angular con respecto a un eje de cuantización.
- Además, en los campos potenciales donde V(x)=V(-x), las funciones propias presentan la propiedad de la paridad, que es un número cuántico que se basa en el comportamiento de la función de ondas respecto a la inversión de todas las coordenadas en relación al origen.
Como curiosidad, la formulación moderna de la ecuación de Schrödinger luce así:

Si resolvemos la ecuación de Schrödinger para el caso concreto del átomo de hidrógeno, constituido por un protón y un electrón, aparecen varias familias de soluciones clasificadas por los números cuánticos ya mencionados:
- n: Número cuántico principal. Determina la energía en el átomo de hidrógeno y el número de nodos radiales de la función de onda.
- l: Número cuántico azimutal (o de momento angular orbital). Relacionado con la forma del orbital. l puede tomar valores desde 0 hasta n−1.
- m: Número cuántico magnético. Indica la orientación del momento angular respecto a un eje de cuantización, con valores enteros entre −l y l.
Estos números cuánticos describen órbitas probables para el electrón (llamadas orbitales atómicos), no trayectorias clásicas. La denominación tradicional de estos orbitales (s, p, d, f…) surge de la forma de la función de onda y la distribución de probabilidad en el espacio. De modo que cada combinación (n,l,m) da lugar a una distribución espacial característica de la función de onda. Para:
- l=0 (orbitales “s”), la nube electrónica es esférica y no depende de los ángulos.
- l=1 (orbitales “p”), aparecen lóbulos bilaterales con diferentes orientaciones según mmm.
- l=2 (orbitales “d”), se presentan distribuciones más complejas con varios lóbulos.
- l=3 (orbitales “f”), la forma es aún más intrincada, y así sucesivamente.
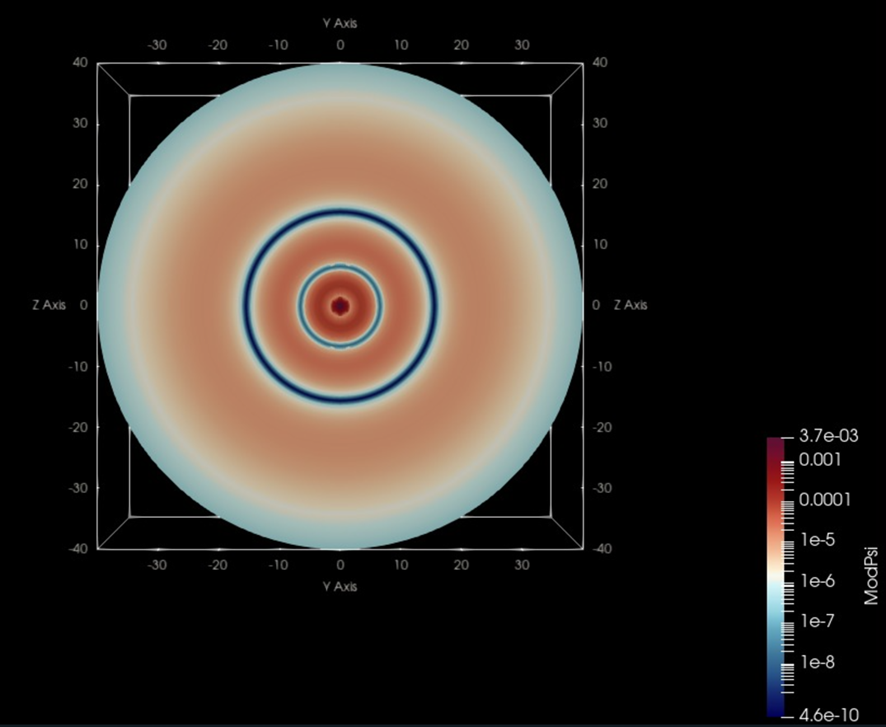
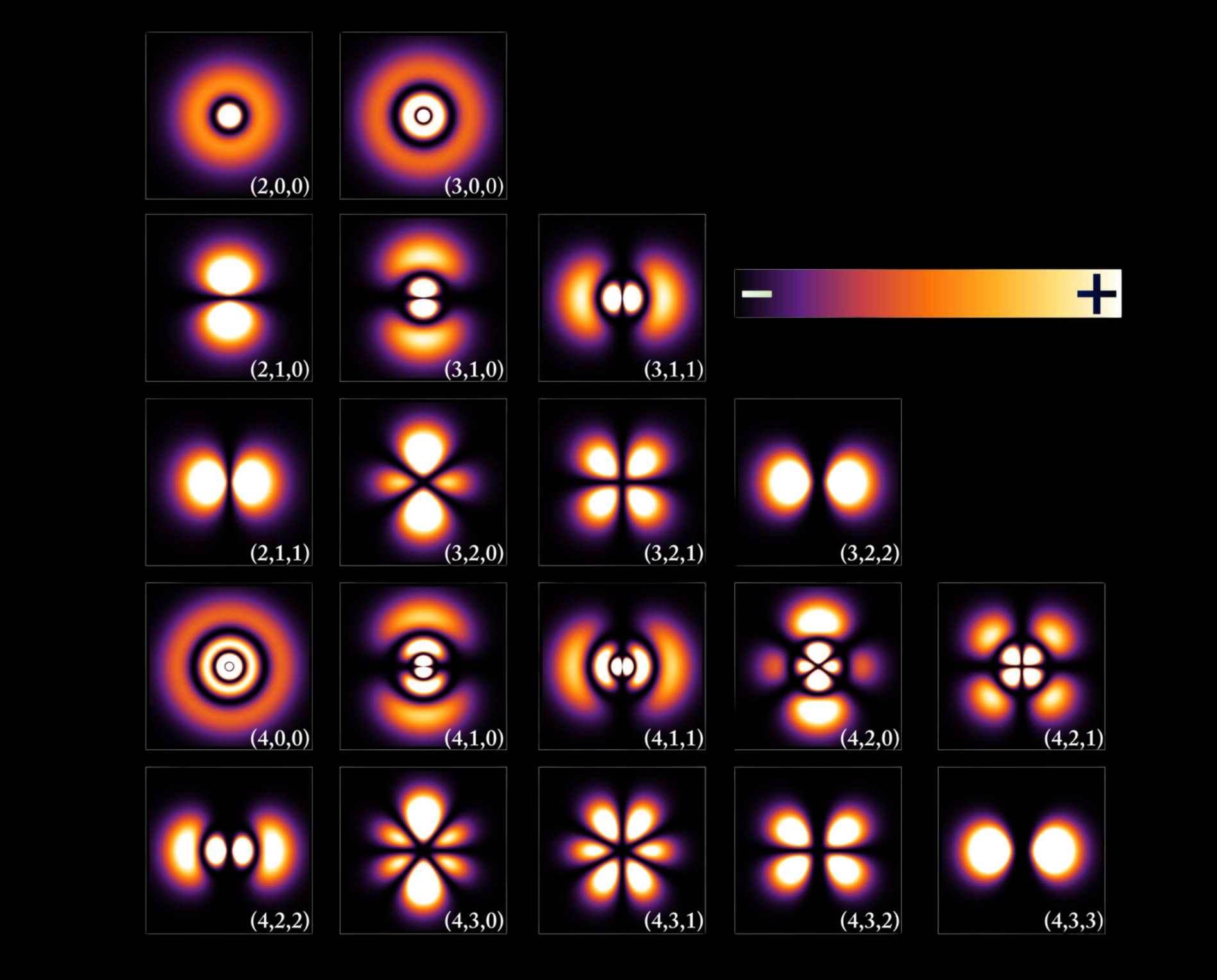
La mecánica cuántica no puede predecir la trayectoria exacta de un electrón, sino la probabilidad de encontrarlo en distintas regiones del espacio. Las zonas en que la función de onda tiene un valor mayor indican alta probabilidad de localizar al electrón; estas zonas se representan a menudo con colores más intensos o con mayor densidad en gráficas tridimensionales. Por ejemplo, en imágenes de los orbitales 1s, 2p, 3d… del hidrógeno, se aprecian anillos o lóbulos que ilustran regiones de mayor o menor probabilidad.
Funciones de onda del electrón en un átomo de hidrógeno a diferentes niveles de energía. La mecánica cuántica no puede predecir la localización exacta de una partícula en el espacio, sólo la probabilidad de encontrarla en diferentes localizaciones. Las zonas más brillantes representan una mayor probabilidad de encontrar el electrón.
Con la intención de arrojar algo de luz a este basto campo de investigación, daremos unas breves pinceladas a estos diferentes nuevos grupos de partículas.
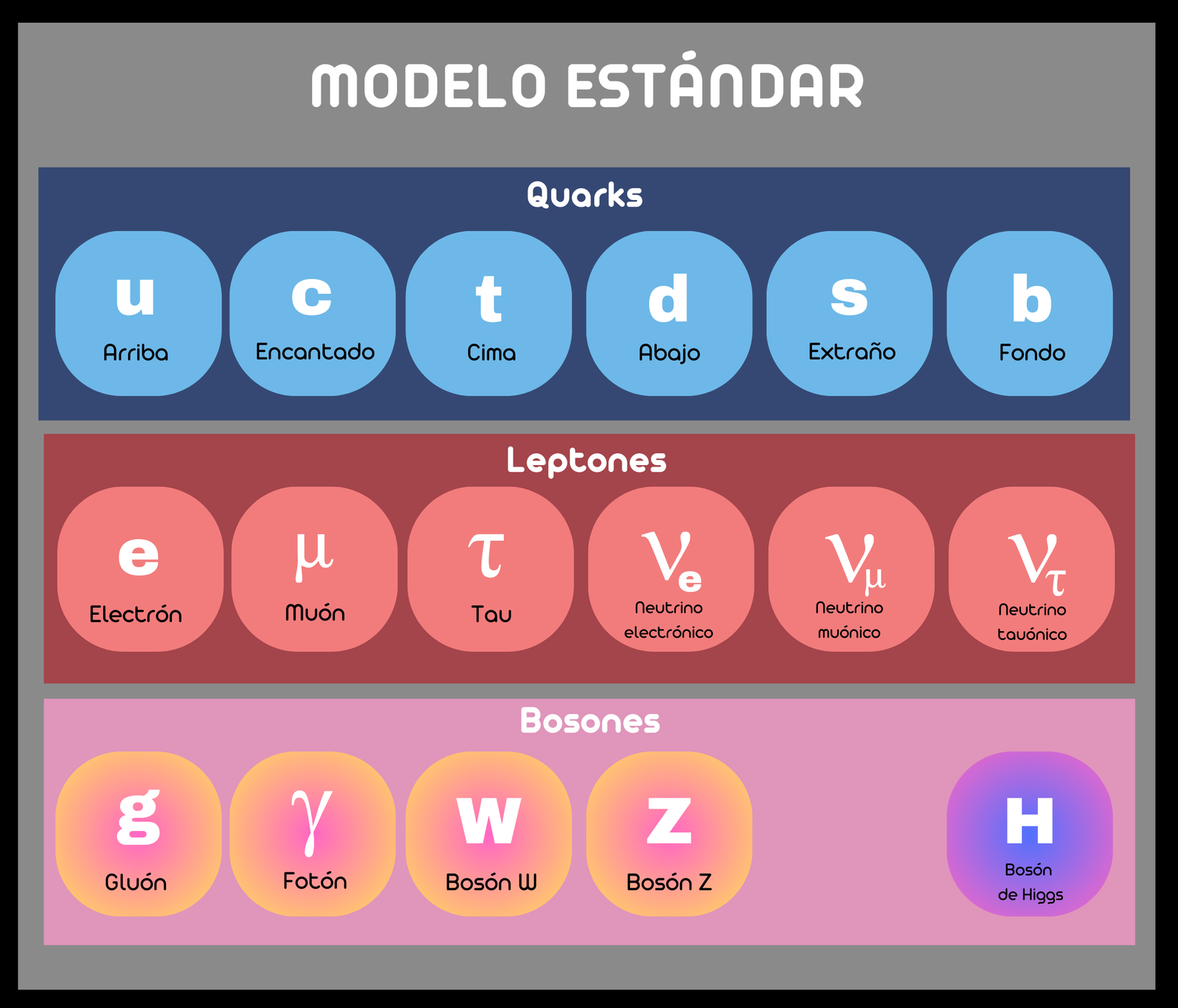
Para ello conviene acudir al Modelo Estándar, que a día de hoy sigue siendo la descripción más completa y aceptada para dar explicación a la mayor parte de fenómenos observados. El Modelo Estándar es el conjunto del modelo quark, la teoría electrodébil y la cromodinámica cuántica, siendo las partículas fundamentales los leptones y los quarks. El Modelo Estándar es capaz de describir las partículas fundamentales y tres de las cuatro interacciones básicas (electromagnética, débil y fuerte) de manera extraordinariamente precisa. Desde su origen hasta nuestros días, ha sido corroborado con gran precisión en innumerables experimentos, por lo que se le considera la teoría vigente en el ámbito de la física de partículas.
A continuación se dará una breve introducción a dos conceptos clave para entender el funcionamiento de la física de partículas: el espín y las antipartículas.
Espín
Una característica importante de una partícula es el espín. En el contexto de la mecánica cuántica, el espín es una propiedad intrínseca de las partículas subatómicas que puede entenderse, de manera simplificada, como una forma de “momento angular interno”. A diferencia de la noción clásica de un objeto girando sobre su eje (rotación física), en el ámbito cuántico el espín no puede interpretarse literalmente como una partícula dando vueltas en el espacio. Más bien, es un grado de libertad fundamental que determina, entre otras cosas, cómo la partícula interactúa con campos electromagnéticos y con otras partículas. Entre sus propiedades se pueden mencionar las siguientes:
- El espín se cuantiza en múltiplos de ℏ\2.
- El valor del espín determina la estadística cuántica que la partícula obedece.
- El espín se relaciona con propiedades magnéticas. Por ejemplo, el electrón tiene un momento magnético intrínseco asociado a su espín, lo que permite su interacción con campos magnéticos.
- El concepto de espín es esencial para describir la estructura fina de los átomos, el comportamiento de materiales magnéticos, y la formación de estados cuánticos colectivos (como la superconductividad).
Antipartícula
En el marco de la física de partículas, para cada tipo de partícula existe una antipartícula correspondiente. Las antipartículas tienen la misma masa que su partícula “original”, pero poseen ciertas propiedades cuánticas opuestas, como la carga eléctrica o algunos números cuánticos (carga de color, isospín, etc., dependiendo de la partícula en cuestión).
Relación partícula-antipartícula
- Cuando una partícula y su antipartícula se encuentran, pueden aniquilarse, liberando energía (por ejemplo, fotones de alta energía en el caso electrón-positrón).
- Algunas partículas son sus propias antipartículas (como el fotón).
Simetrías y antimateria
- La existencia de antipartículas está relacionada con simetrías fundamentales de la naturaleza, como la simetría carga-paridad-tiempo.
- La antimateria es la materia compuesta por antipartículas. Por ejemplo, antiprotones, antineutrones y positrones pueden formar átomos de antimateria como el anti-hidrógeno.
- Uno de los grandes interrogantes en cosmología es comprender por qué el universo observable está compuesto principalmente de materia y hay tan poca antimateria, pese a que las teorías sugieren que ambas debieron haberse formado en cantidades similares tras el Big Bang.
En esencia, según el modelo estándar de la física de partículas, existen tres grupos principales:
- Fermiones. Son las partículas fundamentales que constituyen la materia. Se caracterizan por tener espín semientero (1/2, -1/2, etc.) y obedecen el principio de exclusión de Pauli, por lo que no pueden ocupar el mismo estado cuántico simultáneamente. A su vez, los fermiones se dividen en:
- Leptones. Son partículas fundamentales que no experimentan la interacción fuerte. Existen seis leptones, organizados en tres pares, aunque se podrían dividir en dos grupos: cargados (electrón, muon y tau), que interaccionan con la fuerza electromagnética, y neutrinos, que sólo interaccionan mediante la fuerza débil y la gravedad.
- Electrón y neutrino electrónico
- Muon y neutrino muónico
- Tau y neutrino tauónico
- Quarks. Son partículas fundamentales que se combinan para formar hadrones, las partículas compuestas que incluyen protones y neutrones. Los quarks son únicos porque experimentan todas las fuerzas fundamentales: fuerte, débil, electromagnética y gravitacional.
- Leptones. Son partículas fundamentales que no experimentan la interacción fuerte. Existen seis leptones, organizados en tres pares, aunque se podrían dividir en dos grupos: cargados (electrón, muon y tau), que interaccionan con la fuerza electromagnética, y neutrinos, que sólo interaccionan mediante la fuerza débil y la gravedad.
Si la combinación resulta con espín semientero, estaríamos ante un barión. Los bariones están formados por tres quarks. La combinación de tres fermiones (quarks) resulta en una partícula con espín semientero (por ejemplo, 1/2 o 3/2). Existen seis sabores de quarks, que se agrupan en pares:
- Quark up (u) y quark down (d)
- Quark strange (s) y quark charm (c)
- Quark bottom (b) y quark top (t)
- Bosones. Los bosones son partículas mediadoras de las fuerzas fundamentales. A diferencia de los fermiones, los bosones pueden ocupar el mismo estado cuántico, lo que les permite mediar las fuerzas entre partículas. Los bosones tienen espín entero (0, 1, 2, etc.). Existen los siguientes tipos de bosones confirmados:
- Fotón: Mediador de la fuerza electromagnética.
- Gluones: Mediadores de la fuerza fuerte, que mantienen unidos a los quarks dentro de los hadrones.
- Bosones W⁺, W⁻, Z⁰: Mediadores de la interacción débil, responsables de procesos como la desintegración beta.
- Bosón de Higgs (H): Relacionado con el campo de Higgs, que otorga masa a otras partículas fundamentales.
- Mesones: Están formados por un par de quarks, específicamente un quark y un antiquark. Aunque los quarks individuales son fermiones, la combinación de un quark con un antiquark puede resultar en una partícula con espín entero (0 o 1), lo que clasifica a los mesones como bosones.
Por último, los hadrones son partículas compuestas por quarks, que se mantienen unidos gracias a la fuerza nuclear fuerte, y que se clasifican principalmente en dos familias: bariones (sistemas de tres quarks) y mesones (sistemas de un quark y un antiquark).
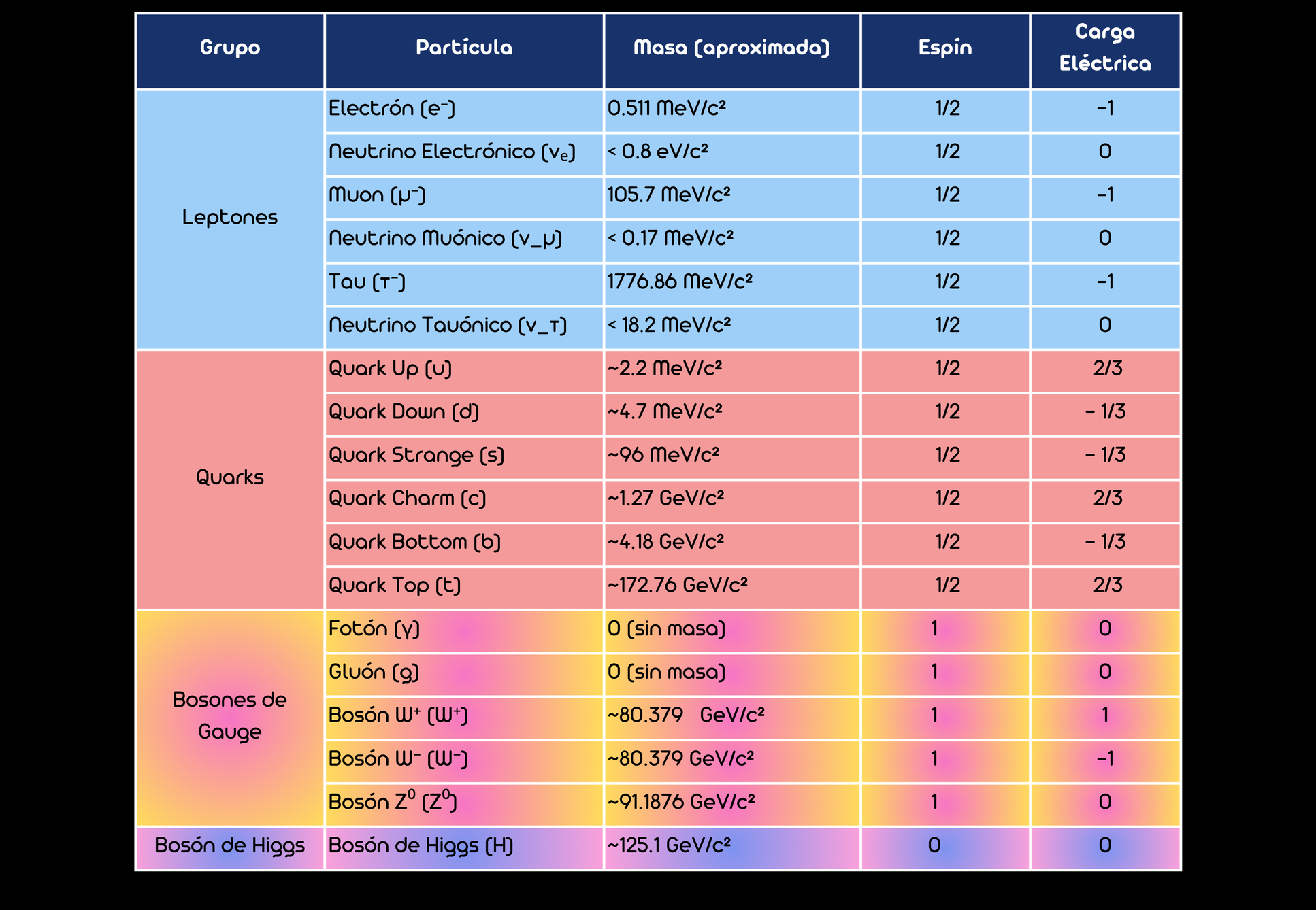
Clasificación general de partículas
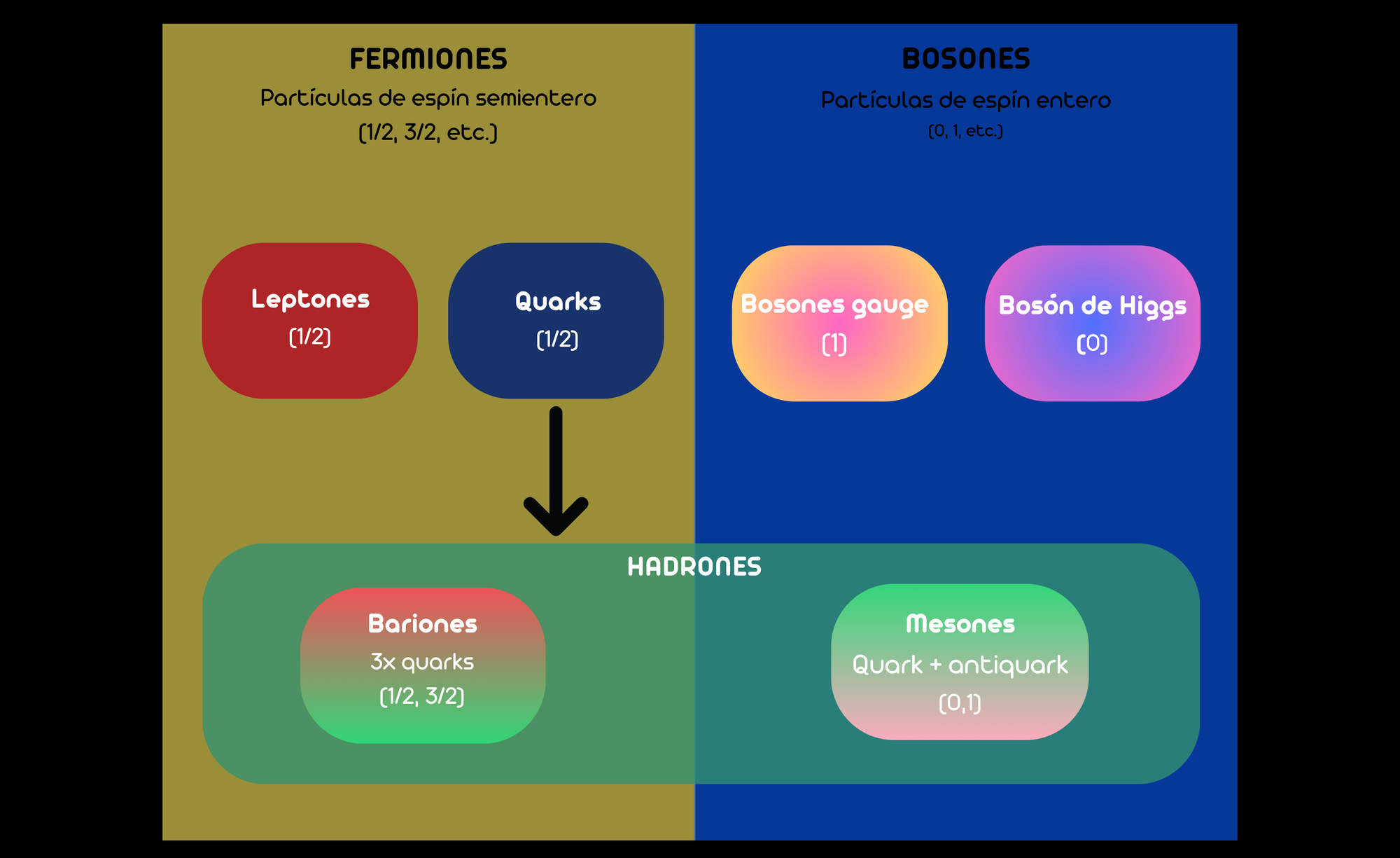
Tabla de partículas fundamentales
Clasificación gráfica de partículas
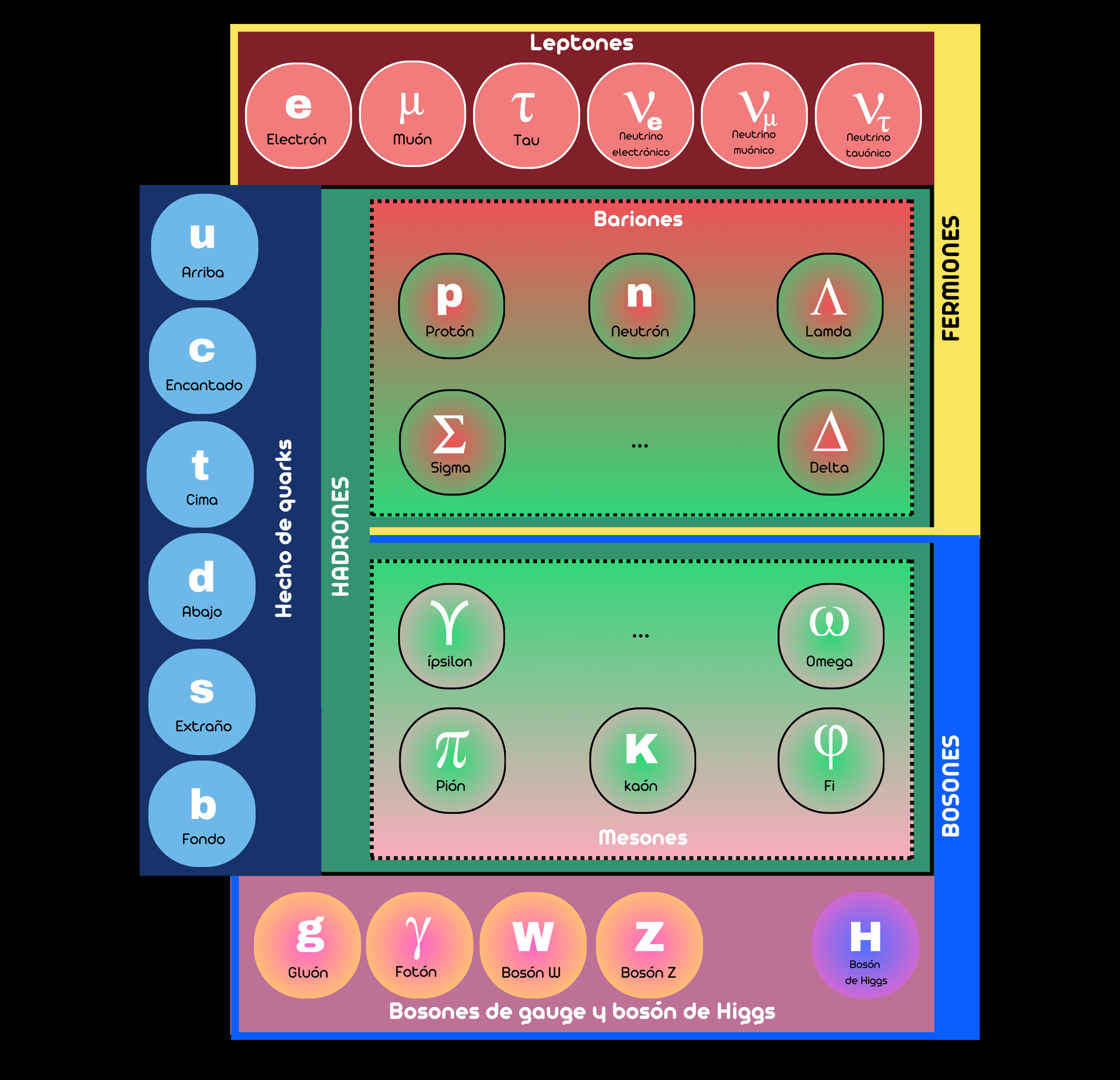
A continuación, y a modo de curiosidad, se facilita un programa en Python que representa los orbitales electrónicos del átomo de hidrógeno. El programa genera una malla vtk con los puntos 3D de los orbitales, y para visualizarlo se requiere el programa Paraview.
"""
Funciones de radial y de onda del átomo de hidrógeno definidas en Python:
"""
import math
import numpy as np
from scipy.special import sph_harm, genlaguerre
def funcion_radial(r, n=1, 1=0):
rho = 2.*r/n
l_poly = genlaguerre(n-l-1,2*l+1)(rho)
normfactor = np.sqrt((2./n)**3*math.factorial(n-l-1)/(2.*n*math.factorial(n+1)))
radial = normfactor* np.exp(-rho/2.)*rho**l* l_poly
return radial
def funcion_onda_hidrogeno(r,theta,phi,n=1,l=0,m=0):
fr = funcion_radial(r,n,l)
s_harm = sph_harm(m,l,phi,theta)
f = fr*s_harm
return f
import numpy as np
import math
from scipy.special import sph_harm, genlaguerre
!pip install vtk
import vtk
def funcion_radial(r, n=1, l=0):
rho = 2.0 * r / n
l_poly = genlaguerre(n - l - 1, 2*l + 1)(rho)
normfactor = np.sqrt((2./n)**3 * math.factorial(n - l - 1)
/ (2.*n * math.factorial(n + l)))
radial = normfactor * np.exp(-rho/2.) * (rho**l) * l_poly
return radial
def funcion_onda_hidrogeno(r, theta, phi, n=1, l=0, m=0):
fr = funcion_radial(r, n, l)
s_harm = sph_harm(m, l, phi, theta)
return fr * s_harm
# --------------------------
# Parámetros de la malla
# --------------------------
rgrid = np.linspace(0.05, 40, 50)
tethagrid = np.linspace(0, np.pi, 50)
phigrid = np.linspace(0, 2*np.pi, 50)
n_r = len(rgrid)
n_theta = len(tethagrid)
n_phi = len(phigrid)
npts = n_r * n_theta * n_phi
# Creamos el StructuredGrid
sgrid = vtk.vtkStructuredGrid()
sgrid.SetDimensions(n_r, n_theta, n_phi)
points = vtk.vtkPoints()
points.SetNumberOfPoints(npts)
# Arrays para almacenar la parte real e imaginaria, y combinada
arrayRe = vtk.vtkFloatArray()
arrayRe.SetName("RePsi")
arrayRe.SetNumberOfValues(npts)
arrayIm = vtk.vtkFloatArray()
arrayIm.SetName("ImPsi")
arrayIm.SetNumberOfValues(npts)
arrayMod = vtk.vtkFloatArray()
arrayMod.SetName("ModPsi")
arrayMod.SetNumberOfValues(npts)
# Pedimos n, l, m
n_escogido = int(input("Número cuántico n: "))
l_escogido = int(input("Número cuántico l: "))
m_escogido = int(input("Número cuántico m: "))
# Recorremos y escribimos, haciendo el correspondiente cambio de coordenadas.
idx = 0
for r in rgrid:
for t in tethagrid:
for p in phigrid:
x = r * np.sin(t) * np.cos(p)
y = r * np.sin(t) * np.sin(p)
z = r * np.cos(t)
points.InsertPoint(idx, x, y, z)
f_complex = funcion_onda_hidrogeno(
r, t, p, n_escogido, l_escogido, m_escogido
)
# Guardamos partes real e imaginaria
arrayRe.SetValue(idx, f_complex.real)
arrayIm.SetValue(idx, f_complex.imag)
arrayMod.SetValue(idx, (f_complex*f_complex.conjugate()).real)
idx += 1
# Asignamos a la malla
sgrid.SetPoints(points)
pdata = sgrid.GetPointData()
pdata.AddArray(arrayRe)
pdata.AddArray(arrayIm)
pdata.AddArray(arrayMod)
# Guardamos fichero
writer = vtk.vtkXMLStructuredGridWriter()
writer.SetFileName(
r'orbitalH.vts'
)
writer.SetDataModeToAscii()
writer.SetInputData(sgrid)
writer.Write()
#Verificamos que se ha llevado a cabo y se ha generado el archivo
print("Archivo .vts escrito.")Ejemplos de lo que puede devolver el programa:
n=1, l=1, m=0
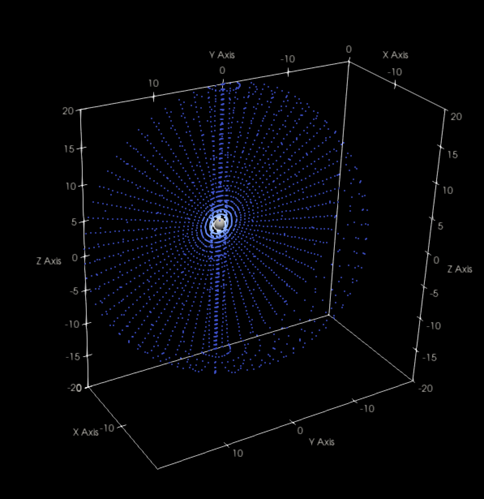
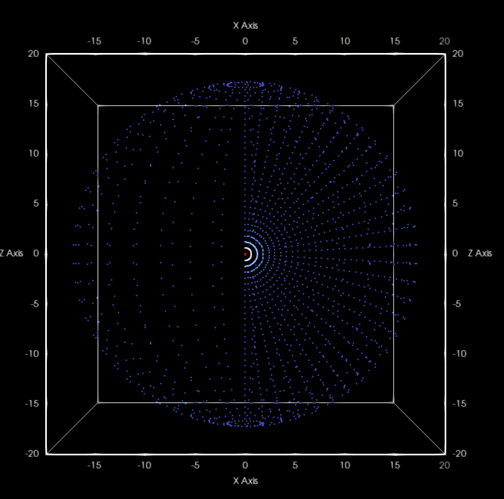
n=2, l=1, m=0
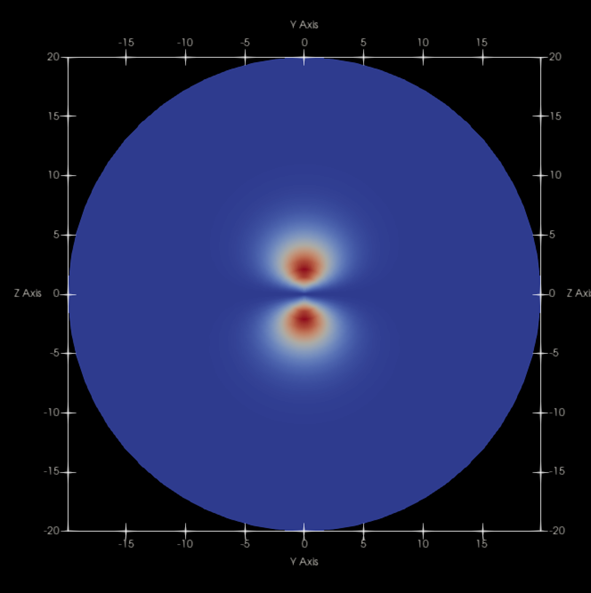
n=4, l=2, m=0
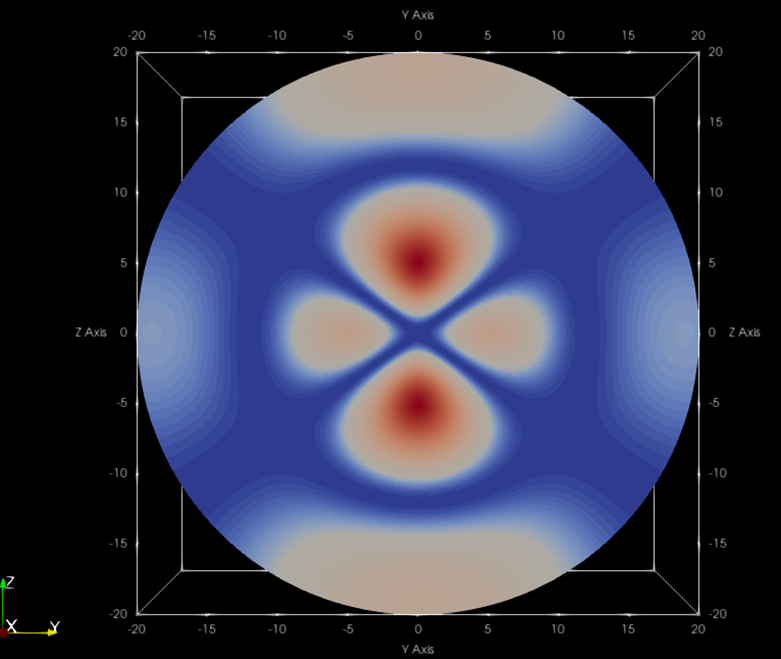
n=4, l=3, m=1
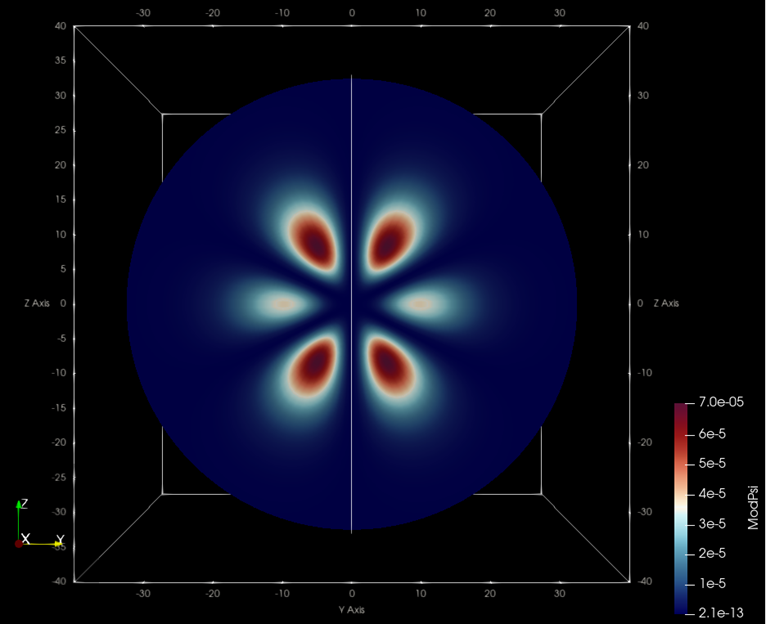
n=4, l=0, m=0