Corrosión: cuando la naturaleza reclama los metales

La corrosión, uno de los grandes enemigos de la ingeniería, es una manifestación más de cómo la naturaleza devuelve las cosas a donde “deberían estar”. Desde que la humanidad aprendió a sustraer los metales de los minerales de la corteza terrestre, tuvo que convivir con este problema. En cierto modo, la corrosión no es más que la tendencia natural de muchos metales a regresar a formas químicas más estables.
No es casualidad que incluso hayamos organizado parte de nuestra historia en torno a los metales.

Clasificación cronológica de las edades del metal basada en los componentes elementales utilizados para la fabricación de objetos en el Mediterráneo oriental y en el sureste de la Península Ibérica. Las composiciones citadas corresponden a aleaciones típicas del sureste de la Península Ibérica.

Traducción de términos:
- B.C.: Antes de Cristo
- Copper Age: Edad del Cobre
- Bronze Age: Edad del Bronce
- Iron Age: Edad del Hierro
- Ancient Age: Edad Antigua
Línea temporal que ilustra el descubrimiento de los metales y las aleaciones, así como algunos acontecimientos clave que han marcado este campo. La línea temporal se divide en dos partes; la parte inferior muestra la evolución entre el 9000 a. C. y el 1700 d. C., incluyendo la Edad de Piedra y la Edad del Bronce. La línea temporal superior muestra los hitos en la investigación sobre metales fusibles y metales líquidos entre el año 1700 d. C. y aproximadamente el año 2000 d. C. En esta segunda línea temporal, los descubrimientos de metales puros y algunos acontecimientos importantes se indican debajo de la línea temporal, mientras que el descubrimiento o la primera descripción de una aleación se indica encima de la línea temporal.
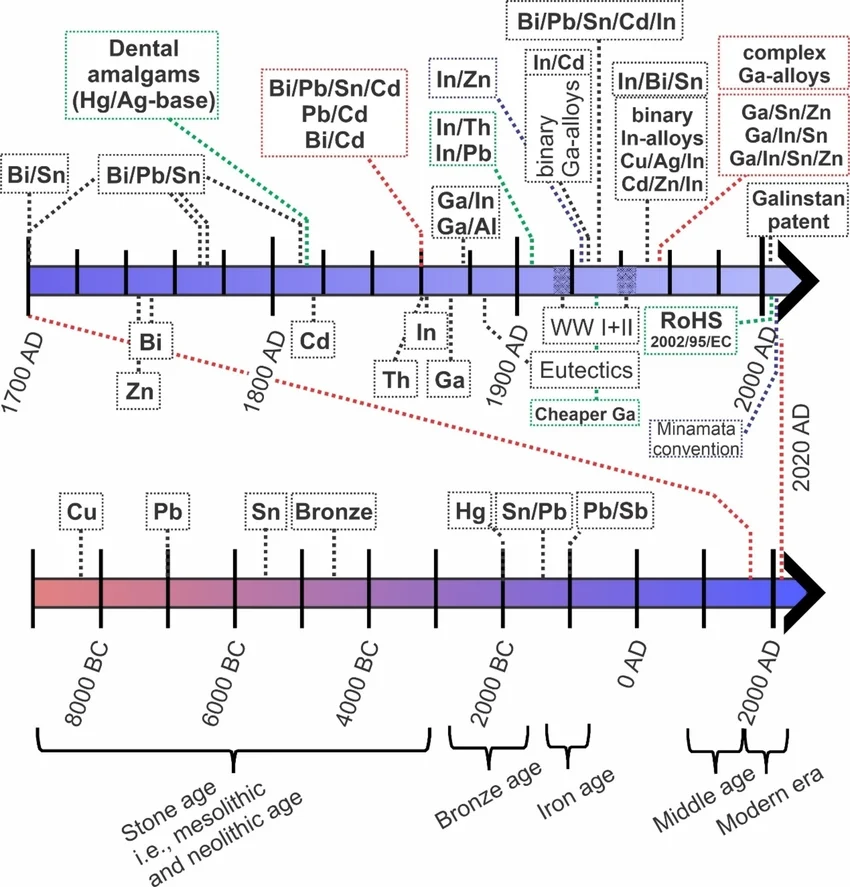
Hablamos de la Edad del Cobre, la Edad del Bronce o la Edad del Hierro porque estos materiales no sólo transformaron herramientas, armas o estructuras, sino que redefinieron civilizaciones enteras. Precisamente por eso, entender la corrosión también es entender uno de los grandes límites materiales a los que la humanidad se ha enfrentado desde sus inicios tecnológicos.
Entonces, ¿cómo podría definirse la corrosión?
La corrosión es el proceso por el cual un material, normalmente un metal, se degrada al reaccionar con su entorno. En la práctica, suele implicar una transformación química o electroquímica hacia un estado más estable, como óxidos, hidróxidos, sulfuros u otras sales.
Conviene resaltar que la corrosión no es únicamente óxido…

Este quizá es el caso más conocido, el típico óxido de hierro que genera esa herrumbre, pero realmente el fenómeno es mucho más amplio. La corrosión puede afectar a:
- aceros y fundiciones
- aluminio
- cobre y sus aleaciones
- zinc
- magnesio
- níquel
- incluso materiales no metálicos, aunque ahí suele hablarse más de degradación química que de corrosión en sentido estricto
La degradación implica un deterioro en las propiedades físicas del material, que puede deberse a factores como el debilitamiento del material por la pérdida de área transversal, a la fractura de un metal por fragilización por hidrógeno o al agrietamiento de un polímero por la exposición a la luz solar.
En muchos casos, la corrosión es un proceso electroquímico, es decir, aparecen zonas donde el metal se oxida y otras donde se produce una reacción de reducción, con transferencia de electrones.
Conviene destacar que en el caso de los metales, se corroen porque son empleados en entornos en los que son químicamente inestables. En la naturaleza sólo el cobre y los metales preciosos como el oro, la plata o el platino se encuentran en estado metálico. Todos los demás metales, entre ellos el hierro (material más empleado), se obtienen a partir de minerales o menas.

Naturaleza electroquímica de la corrosión: reacciones redox
En todo proceso electroquímico, los electrones se transfieren de una sustancia química a otra mediante una reacción de oxidación-reducción o redox. En este tipo de reacción, una especie pierde electrones y otra los gana.
La sustancia que pierde electrones se denomina reductor y se oxida durante el proceso. La especie que gana electrones se denomina oxidante y se reduce.
Como no puede existir una reducción sin una oxidación simultánea, una reacción redox puede dividirse en dos semirreacciones: una de oxidación y otra de reducción.
Por ejemplo, para la reacción entre zinc y bromo:
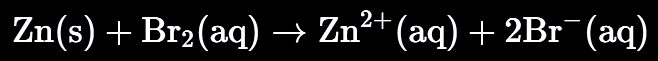
Las semirreacciones son:
Reducción:
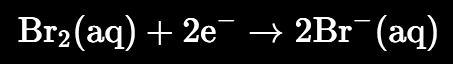
Oxidación:
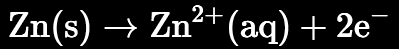
En este caso, el zinc actúa como reductor porque pierde electrones, mientras que el bromo actúa como oxidante porque los gana.
Al sumar ambas semirreacciones se obtiene la reacción global. Para que una reacción redox esté correctamente ajustada, el número de electrones perdidos por el reductor debe ser igual al número de electrones ganados por el oxidante. Además, como en cualquier ecuación química ajustada, la carga neta debe ser la misma en ambos lados de la reacción.
En muchas reacciones químicas, los reactivos suelen estar en contacto físico directo, por ejemplo en una disolución. Sin embargo, en las reacciones redox es posible separar espacialmente la oxidación y la reducción, siempre que exista un circuito cerrado que permita el flujo de electrones entre ambas zonas.
A medida que la reacción avanza, los electrones pasan desde el reductor hacia el oxidante a través de una conexión externa, como un cable, generando una corriente eléctrica que puede utilizarse para realizar trabajo. El dispositivo que permite obtener electricidad a partir de una reacción redox espontánea, o bien usar electricidad para forzar una reacción redox no espontánea, se denomina celda electroquímica.
Existen dos tipos principales de celdas electroquímicas:
- Celda galvánica o voltaica: aprovecha la energía liberada por una reacción redox espontánea para generar electricidad. En este caso:
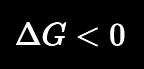
- Celda electrolítica: consume energía eléctrica procedente de una fuente externa para provocar una reacción redox no espontánea. En este caso:
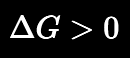
Ambas celdas poseen dos electrodos conectados a un circuito externo. La oxidación ocurre en el ánodo, mientras que la reducción ocurre en el cátodo. Cuando el circuito se cierra, los electrones fluyen desde el ánodo hacia el cátodo.
Además, los electrodos están conectados mediante un electrolito, una sustancia o disolución iónica que permite el movimiento de iones entre las regiones del sistema, manteniendo así la neutralidad eléctrica.
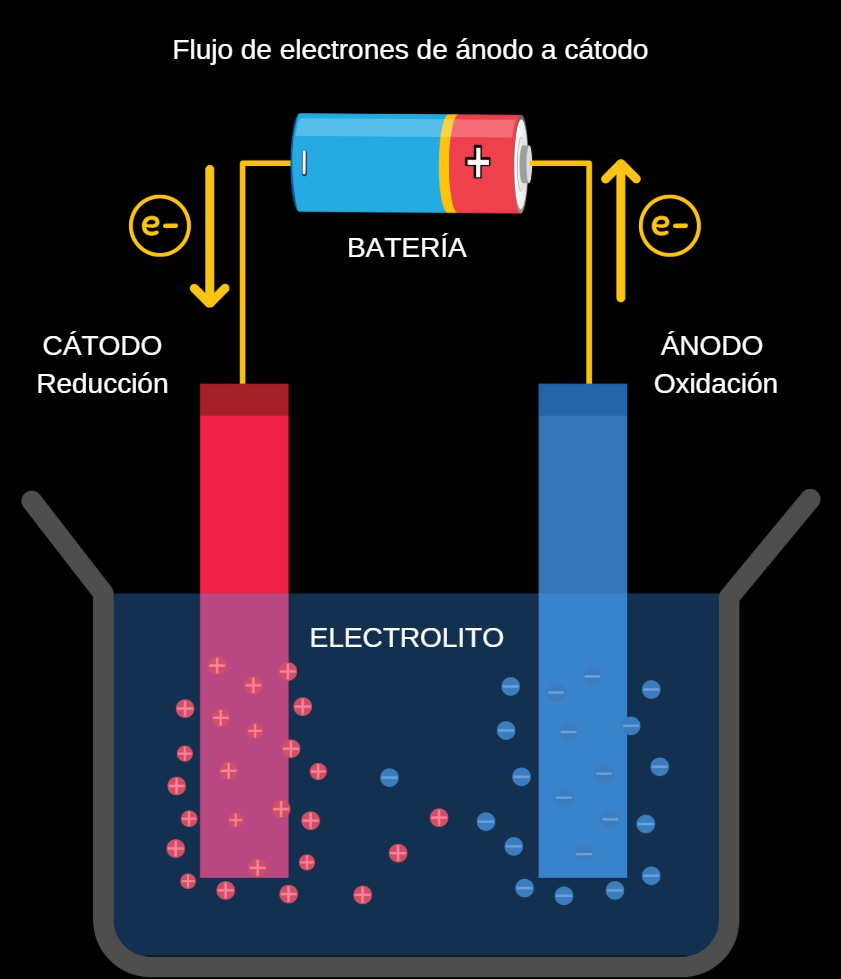
Por lo tanto, en un proceso electroquímico de corrosión suelen intervenir cuatro elementos:
- una zona anódica, donde el metal pierde electrones y se disuelve
- una zona catódica, donde se consume esa carga electrónica
- un camino metálico, por donde circulan los electrones
- un electrolito, como agua con sales, humedad o una disolución conductora
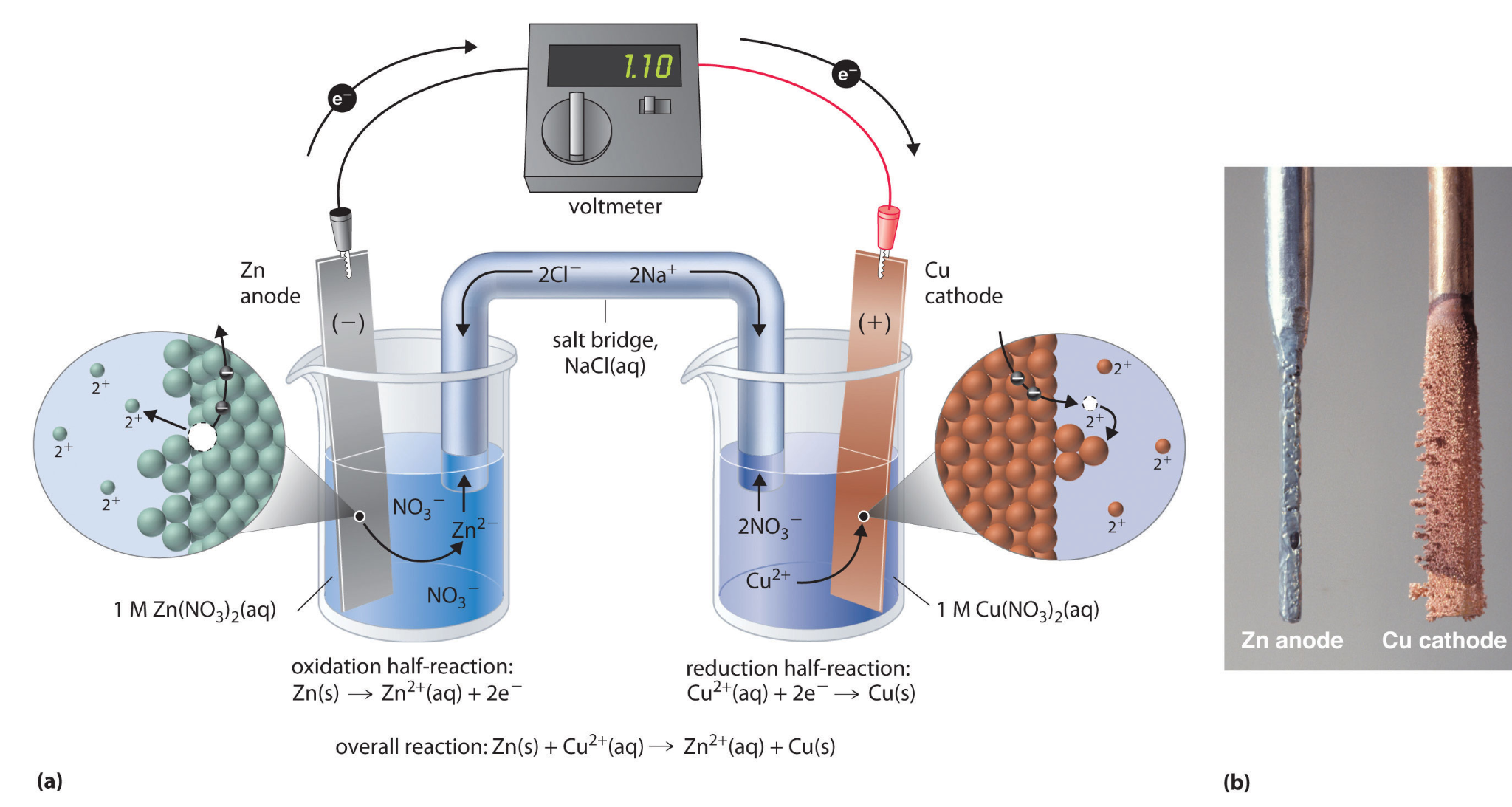
(a) Una celda galvánica puede construirse introduciendo una tira de cobre en un vaso de precipitados que contiene una disolución acuosa 1 M de iones Cu²⁺, y una tira de zinc en otro vaso de precipitados que contiene una disolución acuosa 1 M de iones Zn²⁺. Las dos tiras metálicas se conectan mediante un cable que permite el flujo de electricidad, y los vasos se conectan mediante un puente salino. Cuando se cierra el interruptor para completar el circuito, el electrodo de zinc —el ánodo— se oxida espontáneamente a iones Zn²⁺ en el compartimento izquierdo, mientras que los iones Cu²⁺ se reducen simultáneamente a cobre metálico en el electrodo de cobre —el cátodo—.
Ejemplo típico de oxidación en hierro:
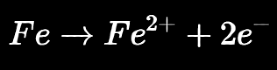
y en aluminio:
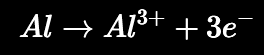
Ejemplos de reducción:
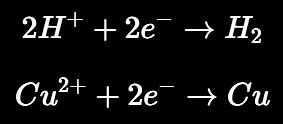
Cátodo en medio aireado y neutro
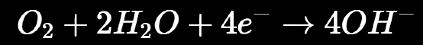
Luego los productos reaccionan y terminan formando óxidos e hidróxidos de hierro.

Factores que favorecen la corrosión
La corrosión depende mucho del entorno. Entre los factores más importantes están:
- humedad
- oxígeno
- sales disueltas, especialmente cloruros
- pH
- temperatura
- velocidad del fluido
- heterogeneidades del material
- tensiones residuales
- diseño geométrico
- contacto entre metales distintos
Un detalle importante es que muchas veces no falla el material “por ser malo”, sino por una combinación errónea de material + ambiente + diseño + fabricación.

Tipos principales de corrosión
1. Corrosión uniforme o generalizada
Es la más “homogénea”. El material va perdiendo espesor de manera más o menos regular en toda la superficie expuesta.
Características:
- es la más fácil de detectar
- suele ser la más fácil de predecir
- a veces, aunque parezca grave, es menos peligrosa que otras formas localizadas
Ejemplo: una chapa de acero que se oxida de forma bastante repartida.

2. Corrosión galvánica
Ocurre cuando dos metales distintos están en contacto eléctrico y además existe un electrolito. El metal menos noble actúa como ánodo y se corroe más rápido.
Ejemplo clásico:
- aluminio unido a acero inoxidable en ambiente marino
- zinc protegiendo al acero
Punto importante: no basta con juntar dos metales; hace falta además un medio conductor, como humedad o agua salina.
Curiosidad: este principio se aprovecha a propósito en la protección catódica con ánodos de sacrificio.

A continuación se muestra una tabla, a modo de matriz de compatibilidad galvánica entre metales. Sirve para estimar, de forma rápida, el riesgo de corrosión galvánica cuando dos materiales metálicos distintos están en contacto eléctrico y, además, comparten un electrolito, como agua, humedad, agua salina o condensación.
Los materiales aparecen ordenados según su nobleza electroquímica: hacia la zona del zinc y del acero galvanizado se sitúan los metales más anódicos o menos nobles, mientras que hacia el níquel y el acero inoxidable se encuentran los más catódicos o más nobles. Cuando se acoplan dos metales alejados en esta serie, el menos noble tiende a actuar como ánodo y se corroe preferentemente, mientras que el más noble actúa como cátodo y queda relativamente protegido.
La leyenda de colores permite interpretar el riesgo del par metálico: las casillas verdes indican que la acción galvánica es insignificante; las naranjas, que puede producirse corrosión galvánica dependiendo del ambiente y de la geometría; y las rojas, que la acción galvánica es probable o esperable. Por ejemplo, combinar zinc o acero galvanizado con cobre, níquel o acero inoxidable implica un riesgo elevado para el metal menos noble, mientras que combinaciones entre materiales próximos en la serie suelen ser más seguras.
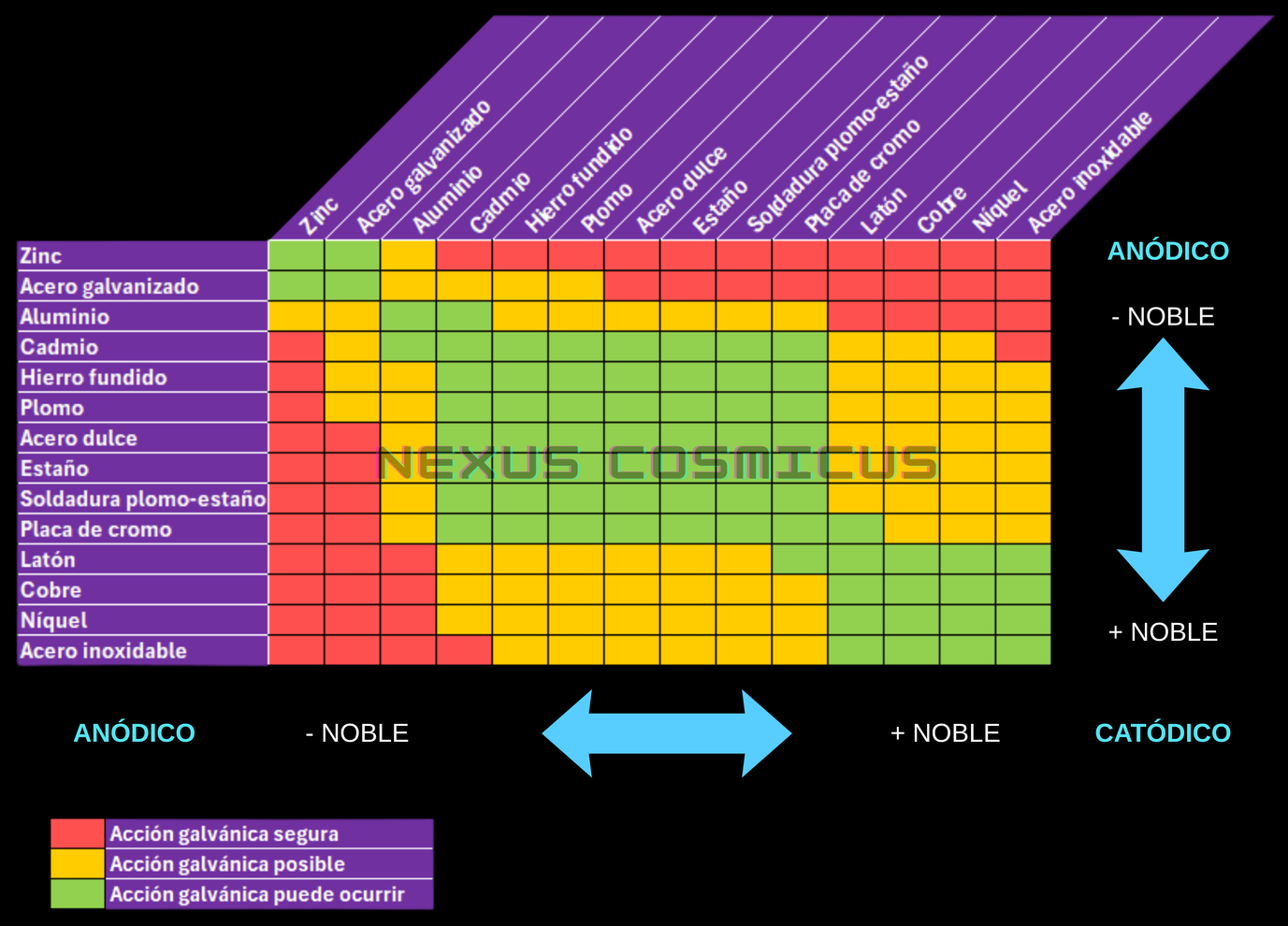
Conviene recordar que la tabla es una guía cualitativa, y no sirve como regla absoluta. El daño real depende de factores como la conductividad del electrolito, la temperatura, la presencia de oxígeno, el área relativa entre ánodo y cátodo, los recubrimientos superficiales y el tiempo de exposición. Un caso especialmente desfavorable es el de un ánodo pequeño unido a un cátodo grande, porque la corriente galvánica se concentra sobre poca superficie y la corrosión del metal menos noble puede acelerarse mucho.
3. Corrosión por picadura
Es una de las más traicioneras, ya que produce ataques muy localizados, pequeños agujeros o cavidades, mientras gran parte de la superficie parece sana.
Es típica en:
- aceros inoxidables
- aluminio
- materiales pasivables
Suele verse favorecida por:
- cloruros
- agua de mar
- rotura local de la capa pasiva
Es peligrosa porque:
- cuesta detectarla
- perfora rápido
- una pérdida de masa pequeña puede causar un fallo grande

4. Corrosión en rendijas
Aparece en zonas estrechas donde el medio queda estancado:
- juntas
- solapes
- bajo arandelas
- uniones atornilladas
- debajo de depósitos o incrustaciones
Aquí el problema reside en que dentro de la rendija cambia la química local: baja el oxígeno, cambian el pH y la concentración de iones, y eso favorece la corrosión localizada.


Crédito imagen: https://armoloy.com/crevice-corrosion-causes-stages-prevention/
5. Corrosión intergranular
Ataca preferentemente los límites de grano del material.
Suele relacionarse con:
- ciertos tratamientos térmicos
- precipitación de fases en borde de grano
- empobrecimiento local en elementos protectores, como el cromo en algunos inoxidables
El resultado puede ser de gravedad, puesto que el componente conserva una apariencia externa aceptable, pero pierde cohesión interna.
6. Corrosión bajo tensión
También llamada stress corrosion cracking cuando hay fisuración. Es la combinación de:
- un material susceptible
- un ambiente específico
- tensiones mecánicas, aplicadas o residuales
Puede generar grietas con muy poca deformación aparente. Es especialmente peligrosa porque puede provocar fallos súbitos.

Microestructura del agrietamiento por Corrosión Bajo Tensión.

7. Corrosión-fatiga
Es la interacción entre un medio corrosivo y cargas cíclicas. El ambiente acelera la iniciación y propagación de grietas por fatiga.
En otras palabras: una pieza sometida a ciclos dura menos en ambiente corrosivo que en aire seco.

8. Erosión-corrosión
Aquí se combinan la corrosión química/electroquímica y el desgaste mecánico por un fluido en movimiento, a veces con partículas.
Es frecuente en:
- tuberías
- codos
- bombas
- válvulas
- intercambiadores de calor
El flujo elimina capas protectoras y deja el metal fresco expuesto.

9. Corrosión selectiva
La corrosión selectiva es un tipo de corrosión en el que uno de los elementos de una aleación se disuelve preferentemente, mientras que el resto del material queda aparentemente intacto. Es decir, no se degrada todo el metal de forma uniforme, sino que el medio corrosivo “extrae” selectivamente uno de sus componentes.
Un ejemplo clásico es la deszincificación de los latones. El latón es una aleación de cobre y zinc. En ciertos ambientes, especialmente aguas estancadas, aguas con cloruros o medios ligeramente ácidos, el zinc puede disolverse preferentemente:
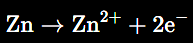
Como resultado, queda una estructura empobrecida en zinc y enriquecida en cobre, normalmente porosa, frágil y con una coloración más rojiza. La pieza puede conservar su forma externa, pero ha perdido buena parte de su resistencia mecánica.

También puede darse un fenómeno similar en fundiciones grises, conocido como grafitización. En este caso, el hierro de la matriz metálica se corroe selectivamente y queda una red de grafito. Visualmente la pieza puede parecer entera, pero mecánicamente se vuelve débil y quebradiza.
Lo peligroso de la corrosión selectiva es precisamente que puede ser poco evidente a simple vista. A diferencia de una corrosión uniforme, donde la pérdida de material es más fácil de estimar, aquí el componente puede mantener su geometría externa mientras su microestructura interna se degrada. Por eso es especialmente problemática en válvulas, racores, tuberías, accesorios de latón, componentes marinos, intercambiadores de calor y sistemas de conducción de agua.
En términos electroquímicos, la corrosión selectiva se debe a diferencias de potencial entre los elementos de la aleación o entre fases metalúrgicas distintas. El elemento menos noble tiende a comportarse como zona anódica y se disuelve preferentemente, mientras que el elemento más noble queda relativamente enriquecido.
10. Corrosión microbiológicamente influida (MIC)
La corrosión microbiológicamente influida o MIC (Microbiologically Influenced Corrosion) es una forma de degradación en la que intervienen microorganismos vivos, como bacterias, hongos o algas, capaces de alterar las condiciones químicas de una superficie metálica y favorecer su deterioro. Aunque estos organismos no siempre “corroen” el metal de forma directa, sí pueden acelerar o desencadenar procesos electroquímicos que terminan incrementando notablemente la velocidad de corrosión.
Este fenómeno suele estar asociado a la formación de biopelículas sobre la superficie del material. En esas películas biológicas, los microorganismos se adhieren, se reproducen y generan un microambiente distinto al del medio circundante. Como resultado, pueden aparecer zonas con diferente concentración de oxígeno, variaciones locales de pH o acumulación de compuestos agresivos, creando las condiciones ideales para que se desarrollen pilas de corrosión localizada, muchas veces en forma de picaduras o ataques muy focalizados.
Además, ciertos microorganismos producen sustancias metabólicas que agravan aún más el problema. Algunos generan ácidos, otros intervienen en ciclos del azufre o del hierro, y otros favorecen reacciones redox que modifican la estabilidad de las capas protectoras del metal. En lugar de limitarse a “alimentarse” de los productos de corrosión, muchos de ellos transforman químicamente el entorno, haciendo que el material quede más expuesto al ataque. Por eso, la MIC no debe entenderse solo como una consecuencia biológica pasiva, sino como una interacción compleja entre biología, química y electroquímica.
Entre los géneros microbianos que suelen citarse en este contexto se encuentran Shewanella, Sulfurimonas y Gallionella, entre otros, debido a su capacidad para intervenir en procesos de oxidación o reducción de compuestos presentes en medios acuosos e industriales. Dependiendo del microorganismo y del entorno, la MIC puede afectar a distintos metales, aunque resulta especialmente relevante en aceros y aleaciones empleadas en infraestructuras hidráulicas e industriales.
Es relevante en:
- tuberías
- tanques
- ambientes marinos
- instalaciones industriales

11. Corrosión por productos activados de corrosión (ACP)
En los reactores nucleares, algunos productos de corrosión liberados por tuberías y componentes metálicos pueden ser arrastrados por el refrigerante hasta el núcleo, donde se activan por la radiación neutrónica. Al redepositarse después en otras zonas del circuito, se convierten en una fuente de radiactividad y aumentan las tasas de dosis durante la operación y el mantenimiento.
Algunos de los muchos tipos de corrosión existentes:


Velocidad de corrosión
La velocidad de corrosión permite cuantificar cuánto material se pierde por unidad de tiempo. Uno de los métodos más simples para medir la corrosión consiste en:
- Tomar una pieza limpia de metal o aleación.
- Pesarla antes del ensayo.
- Exponerla durante un tiempo conocido a un medio corrosivo.
- Limpiarla después para retirar los productos de corrosión.
- Volver a pesarla.
- Calcular la pérdida de masa.
La diferencia entre la masa inicial y la masa final permite estimar cuánto material se ha corroído. La expresión que describiría este fenómeno es:
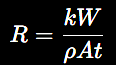
donde:
- R es la velocidad de corrosión.
- W es la pérdida de masa del metal.
- t es el tiempo de exposición.
- A es el área superficial expuesta.
- ρ es la densidad del metal.
- k es una constante de conversión que depende de las unidades empleadas.
Esta fórmula permite convertir una pérdida de masa en una profundidad equivalente de penetración. Es decir, no solo indica cuántos gramos se han perdido, sino cuánto espesor de material se habría consumido si la corrosión fuese uniforme.
En algunos casos, al inicio del proceso, la corrosión u oxidación puede ser rápida, pero después se forma una capa de óxido que actúa como barrera. Entonces, el oxígeno o los iones tienen que difundirse a través de esa capa para seguir reaccionando con el metal, y el proceso se ralentiza.
Esto permite distinguir entre:
- Óxidos protectores, como el óxido de aluminio en el aluminio o la capa pasiva del acero inoxidable.
- Óxidos no protectores, como muchos óxidos de hierro, que pueden agrietarse, desprenderse o permitir que la corrosión continúe.

Fractura bajo corrosión y tensiones
Aunque una superficie metálica pueda parecer homogénea a escala macroscópica, a escala microestructural suele contener heterogeneidades: bordes de grano, segregaciones dendríticas, inclusiones intermetálicas, diferencias de composición, etc. Estas irregularidades pueden actuar como micropilas locales, generando pequeñas zonas anódicas y catódicas. El ataque deja entonces de ser uniforme y se concentra en puntos concretos, dando lugar a una corrosión localizada, más peligrosa que una corrosión generalizada porque favorece la nucleación de grietas.
Además, cuando el material está sometido a tensiones mecánicas, las consecuencias se agravan. Las zonas de máxima tensión favorecen la formación y propagación de defectos, de modo que una picadura, rendija o zona corroída puede comportarse como una entalla mecánica. Esta entalla multiplica localmente la tensión y facilita que el daño avance. Por eso la corrosión puntual o lineal suele ser más crítica que la corrosión superficial generalizada.
También interviene la aireación diferencial: cuando una grieta, rendija o cavidad presenta menor disponibilidad de oxígeno en su fondo que en la superficie exterior, el fondo tiende a comportarse como región más anódica. Esto intensifica el ataque en el interior de la grieta y acelera el deterioro.
La fractura con corrosión aparece cuando el medio ambiente corrosivo actúa conjuntamente con un estado tensional capaz de provocar o acelerar el fallo del material. Se distinguen dos grandes casos:
a) Corrosión bajo tensiones
b) Fatiga con corrosión
La corrosión bajo tensiones se produce cuando un material sometido a tensiones, normalmente estáticas o residuales, se encuentra en un medio corrosivo específico. La corrosión se localiza en el fondo de una grieta inicial y favorece su propagación. Esta propagación puede seguir dos caminos principales:
- Intergranular, avanzando por los bordes de grano.
- Transgranular o transcristalina, atravesando los granos según determinados planos cristalinos.
El mecanismo descrito se basa en la alternancia entre rotura de la película protectora y re-pasivación. Muchos metales forman espontáneamente una capa superficial de óxido que los protege. Sin embargo, en el fondo de una grieta sometida a tensión, los deslizamientos locales pueden romper esa película. Al quedar expuesta una superficie metálica fresca, el medio corrosivo la ataca. Después, la superficie puede volver a pasivarse, pero el proceso se repite: rotura de la película, ataque corrosivo, nueva pasivación y avance de la grieta.
Este mecanismo explica por qué la grieta puede avanzar de forma progresiva aun cuando el material parezca protegido por una película de óxido. La fractura resultante suele presentar baja ductilidad y, en muchos casos, recubrimientos de óxido sobre las superficies de fractura. También pueden aparecer estrías o líneas paralelas a la dirección de propagación de la grieta.
Cálculo del servicio en corrosión bajo tensiones
El cálculo de la corrosión bajo tensiones se relaciona con la mecánica de fractura, y al igual que en la fractura estática, parece existir un valor umbral de multiplicador de tensiones:
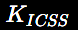
Por debajo de ese valor, las grietas iniciales no avanzan en el medio corrosivo considerado. Por encima, la grieta puede comenzar a propagarse.
El criterio se expresa de forma análoga a la fractura mecánica:

Este valor umbral no depende solo del material, sino también de su estado, sus heterogeneidades y el medio corrosivo de servicio. Por tanto, no es una propiedad universal del material aislado, sino una propiedad del sistema material-medio-condición de servicio.
Generalmente se describen dos etapas en el crecimiento de la grieta:
- Etapa I: crecimiento rápido inicial.
- Etapa II: crecimiento más estable, con velocidad aproximadamente constante, antes de llegar a la fractura final.
El tiempo hasta la fractura total depende inversamente de la velocidad de crecimiento de la grieta. Es decir, cuanto mayor sea la velocidad de avance, menor será la vida útil de la pieza.

Fatiga con corrosión
La fatiga con corrosión aparece cuando un material sometido a cargas cíclicas trabaja en un ambiente corrosivo. En este caso, el efecto de la corrosión se suma al daño por fatiga, reduciendo drásticamente la vida en servicio. Para las condiciones de corrosión se puede emplear también la ecuación de Paris para el cálculo de la fractura en fatiga sin corrosión, que se expresa habitualmente como:

En términos físicos, la ecuación indica que cuanto mayor es la amplitud de carga aplicada a la grieta, mayor es su velocidad de propagación. Se usa sobre todo en la región de crecimiento estable de grieta por fatiga, antes de la fractura final.
Ahora bien, la ecuación de Paris usada para describir el crecimiento de grietas por fatiga, puede extrapolarse a condiciones de corrosión, pero con modificaciones importantes. En particular:
- Aumentan las velocidades de crecimiento de grieta, afectando a los coeficientes C y n de la ley de Paris.
- Desaparece el umbral de fatiga ΔKIS, que en condiciones normales definiría un régimen de vida indefinida.
Esto tiene una consecuencia muy importante: en un medio agresivo no puede asumirse la existencia de un límite de fatiga. Es decir, incluso tensiones cíclicas relativamente bajas pueden acabar produciendo fallo si actúan durante suficiente tiempo en presencia de corrosión.
Además, la corrosión puede seguir actuando durante las paradas de servicio si permanecen tensiones residuales o tensiones de trabajo. Por eso, una pieza puede seguir deteriorándose aunque no esté sometida a ciclos activos de carga en ese momento.
La fatiga con corrosión es especialmente crítica porque reduce la resistencia a fatiga del material, en algunos casos hasta valores muy inferiores a los medidos en aire seco. Conviene matizar que en materiales con baja resistencia a la corrosión, el límite de fatiga en medio corrosivo puede caer incluso a una fracción muy pequeña de la resistencia a tracción.
Corrosión en materiales no metálicos
La corrosión en materiales no metálicos no suele seguir los mismos mecanismos que en los metales. En estos últimos, la corrosión acostumbra a ser un proceso electroquímico, con reacciones de oxidación y reducción. En cambio, en cerámicos y polímeros predominan otros fenómenos.
Corrosión en materiales cerámicos
La mayoría de los materiales cerámicos son muy resistentes a la corrosión. Esto se debe a que sus átomos están unidos mediante enlaces químicos muy fuertes y estables, por lo que su estructura posee poca energía química “disponible” para seguir reaccionando con el entorno. En cierto sentido, puede decirse que muchos cerámicos se encuentran ya en un estado químicamente muy estable, casi como si estuvieran “ya corroídos”.
Cuando un cerámico se degrada químicamente, lo más habitual no es una corrosión electroquímica, sino procesos más simples como:
- disolución del material en un medio agresivo,
- ataque químico directo por reacción con sustancias del entorno,
- o alteraciones superficiales por exposición prolongada a medios ácidos, básicos o a altas temperaturas.
Por tanto, en cerámicos conviene hablar más de ataque químico o disolución que de corrosión en el sentido metálico clásico.
Degradación de polímeros
En los polímeros, el uso del término corrosión es más amplio e impreciso. Su degradación implica procesos fisicoquímicos complejos, muchas veces difíciles de describir con un único mecanismo. No suele tratarse de una corrosión electroquímica, sino de una pérdida progresiva de propiedades por interacción con el ambiente.
A diferencia de muchos materiales de bajo peso molecular, los polímeros suelen ser difíciles de disolver, debido a que sus cadenas tienen una masa molecular muy elevada. Por ello, la disolución completa no es el problema más frecuente, aunque en determinadas aplicaciones sí puede ocurrir. En general, este riesgo puede prevenirse relativamente bien escogiendo el polímero adecuado para el medio de servicio.
Hinchamiento y extracción de aditivos
Un fenómeno muy común en polímeros es el hinchamiento o swelling. Ocurre cuando moléculas pequeñas del entorno penetran en la estructura del polímero. Esto puede producir varios efectos:
- disminución de la rigidez,
- pérdida de resistencia mecánica,
- aumento de volumen,
- cambios dimensionales,
- alteración del comportamiento en servicio.
El proceso inverso también puede ser problemático. Algunos polímeros contienen sustancias añadidas, como plastificantes, para hacerlos más flexibles. Si estos compuestos se pierden por lixiviación o extracción hacia el medio, el material puede volverse más frágil, rígido o quebradizo. Es decir, no solo importa lo que entra en el polímero, sino también lo que sale de él.
Rotura de cadenas poliméricas
El mecanismo de degradación más importante en muchos polímeros es la disminución de la longitud de sus cadenas moleculares. Cuando las cadenas se rompen, el material pierde cohesión y sus propiedades empeoran. Esto puede traducirse en:
- fragilidad,
- pérdida de elasticidad,
- fisuración,
- decoloración,
- envejecimiento prematuro.
Entre los agentes que favorecen esta rotura se encuentran:
- la radiación ultravioleta,
- la radiación ionizante,
- los radicales libres,
- el oxígeno,
- el ozono,
- y agentes oxidantes como el cloro.
Un caso clásico es el agrietamiento por ozono en el caucho natural, donde aparecen grietas superficiales debido al ataque químico de este gas.
Agrietamiento por ozono (ozonolisis) en los tubos de caucho natural
Papel de los aditivos
Muchos polímeros incorporan aditivos estabilizantes para retrasar su degradación. Estos pueden actuar absorbiendo radiación UV, frenando reacciones oxidativas o protegiendo frente al envejecimiento ambiental. A veces basta con añadir pigmentos que también cumplen una función protectora, como el dióxido de titanio y el negro de carbono.
Estos compuestos no solo aportan color, sino que pueden mejorar notablemente la durabilidad del material frente a la luz solar y otros agentes ambientales.
Un detalle interesante es que no siempre se busca maximizar la estabilidad. Por ejemplo, algunas bolsas de plástico de un solo uso pueden fabricarse sin ciertos estabilizantes para facilitar que se fragmenten más rápidamente con la exposición ambiental. El problema es que esa degradación no implica una desaparición real del material, sino su conversión en partículas muy pequeñas, potencialmente problemáticas como residuo.
A grandes rasgos, cuando se habla de corrosión en no metales, conviene distinguir dos grandes comportamientos:
- En los cerámicos, domina la gran estabilidad química, y el deterioro suele darse por disolución o reacción química directa.
- En los polímeros, la degradación suele manifestarse como hinchamiento, pérdida de aditivos, oxidación, fotoenvejecimiento y rotura de cadenas moleculares.
Así, más que una corrosión electroquímica como la de los metales, en los no metálicos suele hablarse de degradación química, fisicoquímica o ambiental.
¿Se puede aprovechar la corrosión?
Aunque solemos presentar la corrosión como un enemigo a evitar, o al menos a mitigar, la realidad, como de costumbre, puede llegar a ser más compleja. La corrosión no siempre es sinónimo de fallo. En determinados casos, si se controla adecuadamente, puede convertirse en una herramienta útil para proteger superficies, modificar propiedades, decorar materiales o incluso fabricar dispositivos funcionales.
La clave está en la diferencia entre una corrosión descontrolada y una corrosión inducida de forma controlada. En el primer caso, el material se degrada de manera progresiva, impredecible y potencialmente peligrosa. En el segundo, se favorece la formación de una capa superficial estable, adherente y relativamente impermeable que actúa como barrera frente al medio exterior.
La corrosión como capa protectora
Muchos metales, al reaccionar con el oxígeno, el agua u otros compuestos del ambiente, forman productos de corrosión sobre su superficie. En algunos casos, esos productos son porosos, frágiles y poco adherentes. Es lo que ocurre, por ejemplo, con la herrumbre del hierro: el óxido formado no protege bien, se desprende con facilidad y permite que el ataque continúe hacia el interior.
Pero otros metales forman capas de óxido muy compactas y adheridas. Estas capas pueden actuar como una especie de “piel” protectora que separa el metal del ambiente. Este fenómeno se conoce como pasivación.
Metales como el aluminio, el titanio o el cromo son especialmente interesantes porque forman películas superficiales de óxido muy estables. De hecho, la resistencia a la corrosión de muchos aceros inoxidables se debe precisamente a la presencia de cromo, que permite formar una fina capa protectora de óxido de cromo sobre la superficie.
En este sentido, la corrosión no desaparece: se detiene a sí misma cuando genera una barrera suficientemente eficaz.
No obstante, conviene matizar que, en este contexto, no cualquier producto de corrosión es beneficioso. Para que una capa oxidada sea protectora debe cumplir varias condiciones:
- debe ser adherente;
- debe ser compacta;
- debe ser relativamente impermeable;
- debe ser estable en el medio de servicio;
- y debe cubrir de forma continua la superficie.
Si la capa se agrieta, se desprende, es porosa o permite el paso de agua, oxígeno e iones agresivos, entonces la corrosión puede continuar por debajo. Este es el problema típico de muchos óxidos de hierro: no forman una barrera suficientemente eficaz y el ataque progresa.
Por eso el diseño de capas protectoras no consiste simplemente en “dejar que el metal se oxide”, sino en controlar qué compuesto se forma, con qué espesor, bajo qué condiciones y sobre qué material.
Anodizado: oxidar para proteger
Uno de los ejemplos más claros de corrosión aprovechada industrialmente es el anodizado. Se trata de un proceso electroquímico mediante el cual se hace crecer de forma controlada una capa de óxido sobre la superficie de un metal, especialmente aluminio, aunque también puede aplicarse a titanio, magnesio u otros metales.
En el anodizado, la pieza actúa como ánodo dentro de una celda electrolítica. Al aplicar una corriente eléctrica, se favorece la formación de una capa de óxido más gruesa, ordenada y controlada que la que se formaría espontáneamente al aire.
En el caso del aluminio, el anodizado produce una capa de óxido de aluminio que mejora la resistencia frente a la corrosión y el desgaste. Además, esa capa puede presentar poros microscópicos que permiten incorporar colorantes, lo que explica su uso en piezas decorativas, carcasas, componentes arquitectónicos, bicicletas, dispositivos electrónicos o elementos aeronáuticos.
En el caso del titanio, el anodizado permite generar capas de óxido de titanio con diferentes espesores. Estos espesores modifican la interferencia de la luz reflejada y pueden producir colores sin necesidad de pigmentos. Además de la función estética, la capa de óxido puede mejorar la biocompatibilidad y la resistencia a la corrosión.
Un ejemplo relevante sería un tornillo de titanio Ti-6Al-4V con recubrimiento de óxido anódico. Esta aleación, muy usada en aplicaciones biomédicas y aeroespaciales, ya presenta una excelente resistencia a la corrosión gracias a la formación natural de óxido de titanio. Sin embargo, mediante anodizado se puede aumentar y controlar esa película superficial, mejorando su comportamiento en ambientes fisiológicos, su integración con tejidos o su identificación visual mediante coloración superficial.
Tornillo de titanio Ti-6Al-4V con recubrimiento de óxido anódico

Pavonado: una oxidación controlada del acero
Otro caso clásico es el pavonado, muy utilizado en aceros. Consiste en generar una capa superficial oscura, normalmente asociada a óxidos de hierro, que proporciona cierta protección frente a la corrosión y un acabado estético característico.
A diferencia de una herrumbre común, que suele ser rojiza, porosa y destructiva, el pavonado busca formar una película más uniforme y adherente. No convierte al acero en inoxidable, pero sí mejora su resistencia frente a la oxidación ligera, sobre todo si se combina con aceites o ceras protectoras.
El pavonado se emplea en herramientas, piezas mecánicas, armas, tornillería, elementos decorativos y componentes donde interesa reducir reflejos, mejorar el aspecto superficial o proporcionar una protección básica frente al ambiente.
Pátinas protectoras: el verde de la Estatua de la Libertad
Uno de los ejemplos más conocidos de corrosión útil es la pátina verde del cobre. La Estatua de la Libertad no “se está pudriendo” por estar verde. Su color no indica necesariamente una degradación catastrófica, sino la formación de una capa superficial de compuestos de cobre generados por la exposición prolongada a la atmósfera.
Originalmente, la Estatua de la Libertad tenía un tono cobrizo. Con el tiempo, el cobre de su superficie reaccionó con el oxígeno, el agua, el dióxido de carbono y contaminantes atmosféricos, formando una pátina verdosa compuesta por distintos óxidos, carbonatos, sulfatos y otros compuestos de cobre.
Esta pátina actúa, en buena medida, como una capa protectora. No es el “blindaje" perfecto, pero sí reduce la velocidad con la que el cobre subyacente sigue reaccionando con el ambiente. Por eso muchas cubiertas, cúpulas y esculturas de cobre adquieren con el tiempo ese tono verde característico sin que ello implique necesariamente una pérdida estructural grave.

Grabado químico: eliminación selectiva
También existen procesos donde la corrosión se aprovecha no tanto para proteger, sino para eliminar material de forma selectiva. Es el caso del grabado químico. En este proceso, una sustancia química ataca determinadas zonas de una superficie mientras otras permanecen protegidas por una máscara, barniz, resina o recubrimiento resistente. Así se pueden generar patrones, relieves, canales, texturas o geometrías muy finas.
El grabado químico se utiliza en metalografía para revelar la microestructura de los materiales. Al atacar preferentemente ciertas fases, bordes de grano o regiones con distinta composición, permite observar al microscopio detalles que de otro modo quedarían ocultos.
También se emplea en microfabricación, electrónica, fabricación de circuitos impresos, decoración de metales y producción de piezas con geometrías delicadas.
Ánodos de sacrificio: dejar que se corroa lo menos importante
Uno de los casos más recurrentes en todo tipo de áreas, es la corrosión aprovechada mediante el empleo de ánodos de sacrificio. Se utilizan para proteger estructuras metálicas más valiosas, como cascos de barcos, tuberías enterradas, depósitos, plataformas marinas o intercambiadores de calor.
El principio sobre el que se sustenta es el que ya hemos visto previamente, electroquímico. Se conecta al metal que queremos proteger otro metal más activo, es decir, con mayor tendencia a oxidarse. Ese metal más activo funciona como ánodo y se corroe preferentemente. Por eso se le llama “de sacrificio”: se destruye él para proteger a la estructura principal.
Materiales como el zinc, el magnesio o el aluminio se utilizan con frecuencia como ánodos de sacrificio. Al oxidarse, suministran electrones a la estructura protegida y reducen su tendencia a actuar como ánodo. La pieza principal queda desplazada hacia un comportamiento más catódico y su corrosión se ralentiza.
Este sistema es una forma de protección catódica. No elimina la corrosión del conjunto, pero la traslada hacia un componente diseñado para ser reemplazado periódicamente.
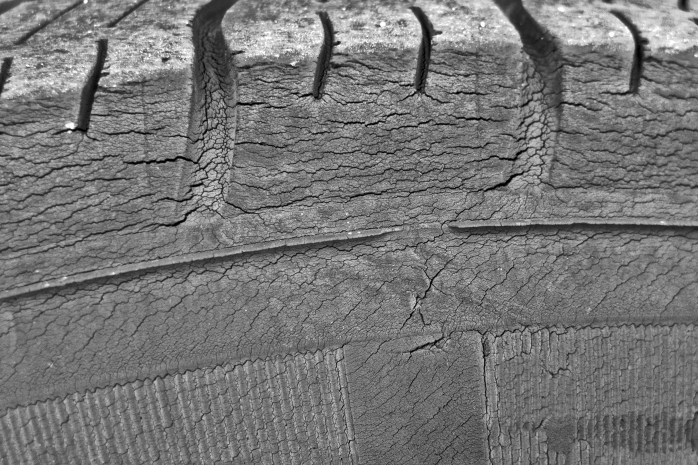
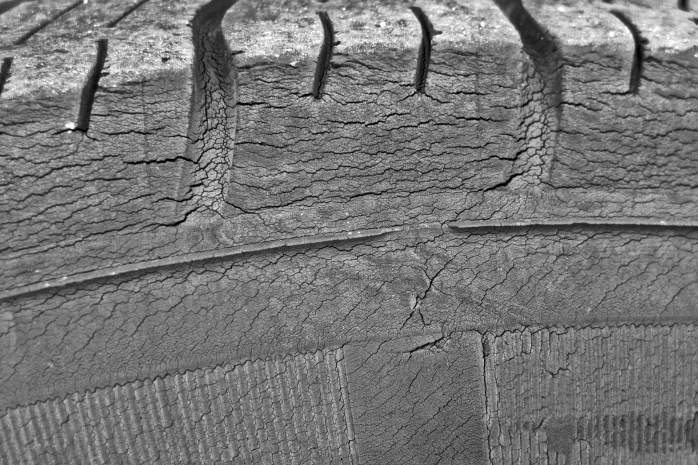
Ejemplo de ánodos de sacrificio en un calentador de agua eléctrico. Generalmente, dentro de los tanques de agua (que contienen sales disueltas) se incorporan ánodos de magnesio que prevén la corrosión de las paredes del tanque y de otros elementos, como los tubos o las resistencias eléctricas.
Antes y después de un ánodo de magnesio empleado en un calentador de agua eléctrico.

Ejemplos de ánodos empleados en el sector naval para proteger el casco de los barcos de la corrosión.

Las pletinas rectangulares que se aprecian en la imagen del timón y la hélice son ánodos galvánicos para salvaguardar la integridad del casco y demás elementos críticos.

La corrosión suele asociarse a pérdida, fallo y deterioro. Y con razón: en puentes, barcos, tuberías, reactores, implantes o estructuras industriales, una corrosión mal controlada puede tener consecuencias graves. Pero desde el punto de vista de la ciencia de materiales, también puede verse como una herramienta.
- Puede proteger, como en el anodizado o las pátinas.
- Puede decorar, como en el pavonado o el titanio anodizado.
- Puede fabricar, como en el grabado químico.
- Y puede sacrificarse de forma inteligente, como en la protección catódica mediante ánodos de sacrificio.
La diferencia está en el control y en la comprensión de los materiales a emplear, así como en el ambiente de operación.
Si bien la corrosión descontrolada puede ser muy destructiva y peligrosa; bien entendida, y dirigida, puede convertirse en una aliada.

Referencias:

https://public.ksc.nasa.gov/corrosion/corrosion-fundamentals/

https://www.fhwa.dot.gov/bridge/nbis/pubs/nhi10029.pdf





https://www-pub.iaea.org/MTCD/Publications/PDF/TE_1672_web.pdf

Ferrer Giménez, C. y Amigó Borrás, V., Tecnología de materiales, Editorial Universitat Politècnica de València,